从手性DMAP到DMAP-N-O带来的新发现
注:文末有本文科研思路分析
酰基转移是自然界和有机合成中常见的转化,其中手性DMAP是常见的不对称酰基转移催化剂。自1996年,Vedejs和Fu小组分别报道中心手性和面手性的DMAP催化剂以来,手性DMAP催化剂得到了极大的发展,各种中心手性、面手性、螺手性和中心手性的DMAP陆续报道,且在许多不对称酰基转移反应中得到了很好的应用。然而,手性DMAP均是以氮作为亲核位点,如果将手性DMAP变为手性DMAP-N-O,其亲核位点就变为氧,将带来新的发现和机遇。
手性催化剂的设计与合成是不对称催化反应研究的核心问题之一。近日,河南师范大学郭海明教授(点击查看介绍)课题组设计合成了一类手性DMAP-N-O酰基转移催化剂,并用于O-酰基吖内酯的不对称Steglich重排反应中,取得了高达97%的ee值。该研究工作以DMAP-N-O的氧为亲核位点,突破了手性DMAP以氮作为亲核位点的思维局限,将为后续手性DMAP-N-O类催化剂的发展奠定基础。
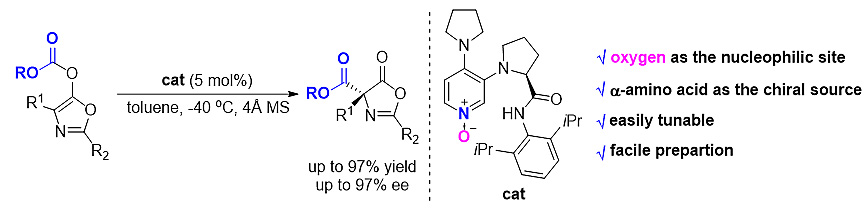
该手性DMAP-N-O酰基转移催化剂,以廉价易得的L-脯氨酸为手性源,在吡啶环的C3位引入L-脯氨酰胺片段,结构易修饰,合成简便,且含有N-H键作为氢键给体。
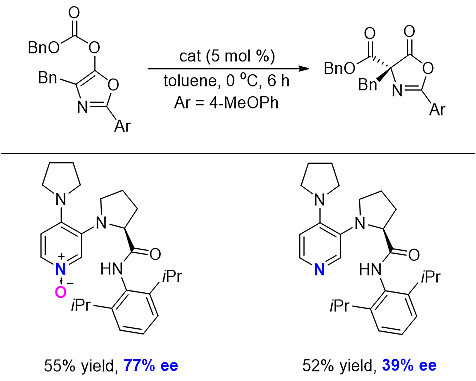
将该手性DMAP-N-O与其还原产物对比,可以发现将手性DMAP变成手性DMAP-N-O可能会对催化效果产生较大的影响。
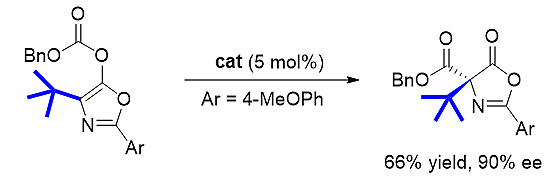
值得一提的是,C4-叔丁基取代噁唑碳酸酯,因其位阻太大,其不对称Steglich重排无人报道。而作者所发展的DMAP-N-O能取得不错结果。
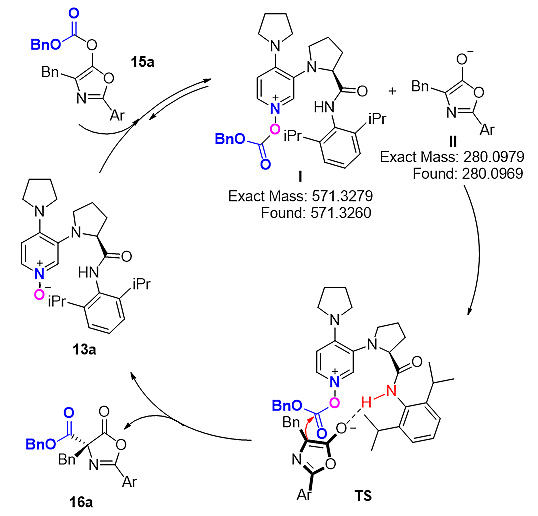
在机理研究方面,通过HRMS分别监测到酰氧基吡啶正离子和吖内酯的烯醇负离子;交叉实验验证了该Steglich重排仍然是分子间酰基转移;将酰胺的N-H进行甲基化后,产物的ee值急剧下降,说明该酰胺N-H起到了氢键给体的作用。基于上述实验和文献中的相关研究,提出了可能的反应机理。
该成果近期发表在Angew. Chem. Int. Ed. 上,文章的实验部分主要由河南师范大学硕士研究生张业飞完成,郭海明教授和谢明胜副教授为共同通讯作者。
该论文作者为:Ming-Sheng Xie,* Ye-Fei Zhang, Meng Shan, Xiao-Xia Wu, Gui-Rong Qu, and Hai-Ming Guo*
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Chiral DMAP-N-oxides as Acyl Transfer Catalysts: Design, Synthesis, and Application in Asymmetric Steglich Rearrangement
Angew. Chem. Int. Ed., 2019, 58, 2839, DOI: 10.1002/anie.201812864
导师介绍
郭海明
https://www.x-mol.com/university/faculty/20138
科研思路分析
Q:这项研究的最初目的是什么?或者说想法是如何产生的?
A:我们在合成手性核苷时,使用了手性DMAP催化剂(Org. Lett., 2018, 20, 1212.)。当时就想设计一种新型手性DMAP催化剂。
根据亲核性顺序:4-吡咯烷基吡啶PPY > DMAP,说明吡咯烷基是强给电子基;3,4,5-三氨基吡啶>PPY,说明C3位氨基也能增强吡啶亲核性。
如果在DMAP的C3位引入强给电子的吡咯烷基,就能进一步增强吡啶的亲核性;而L-脯氨酸中也含有吡咯烷片段,且能与胺反应生成种类多样的L-脯氨酰胺。将两个吡咯烷叠加,就设计出了氨基酸衍生的DMAP催化剂。
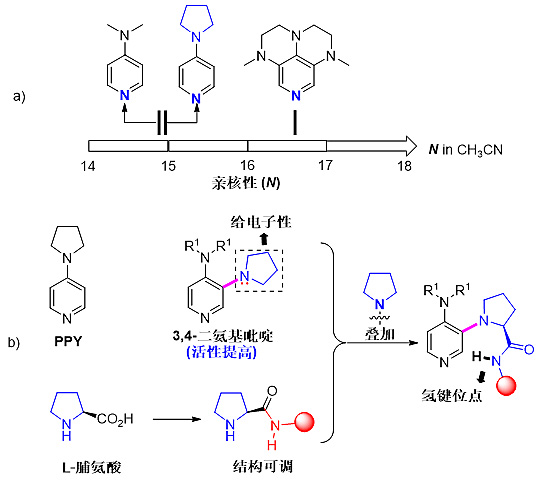
实验过程中,意外发现手性DMAP-N-O能更好催化不对称Steglich重排反应。
Q:意外发现的过程是什么?为什么会用3-溴-4-硝基吡啶氮氧为起始原料?
A:最初我们使用3-溴-DMAP与L-脯氨酰胺偶联,没有产物生成。分析可能原因是:给电子的二烷基氨基使SNAr反应活性更低,且脯氨酰胺的位阻较大。
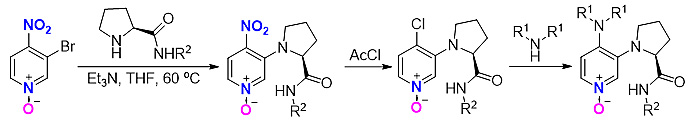
通过查阅文献:3-溴-4-硝基吡啶氮氧,因硝基和氮氧的双重拉电子作用,能够活化C3位的溴。我们以3-溴-4-硝基吡啶N-O与L-脯氨酰胺偶联,再经硝基变氯,可得3-氨基-4-氯吡啶氮氧,再进行还原/胺化或胺化/还原,可得3,4-二氨基DMAP催化剂。
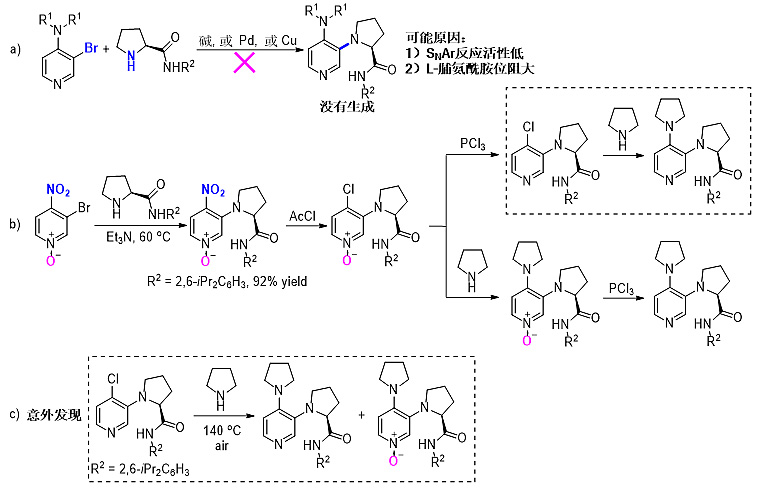
在进行Steglich重排反应的条件筛选时,当使用2,6-二异丙基衍生的DMAP时,其ee值有39%。
有一次实验,ee值出现波动,升高到70% ee。通过对比试验排查出原因是:在3-氨基-4-氯吡啶与吡咯烷反应制备3,4-二氨基吡啶时,由于该反应体系温度较高(140 度、封管反应),反应管中存在空气,使得3,4-二氨基吡啶被部分氧化成3,4-二氨基吡啶氮氧,该催化剂中混有的3,4-二氨基吡啶氮氧使反应ee值升高。
意外发现:3,4-二氨基吡啶氮氧的催化效果更好,能给出77%的ee值。随调整催化剂合成路线,将3-氨基-4-氯吡啶氮氧直接进行胺化反应,可到3,4-二氨基吡啶氮氧,比原设计的手性DMAP的合成路线还缩短了1步。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号