Mater. Today:光镊技术组装手性超构材料
手性是自然界中普遍存在的一种几何构象。如同人类的左右手,手性材料指的是在三维空间中与自身镜像无法重合的物体。在生命科学中,手性更是司空见惯。人体中的许多分子,如氨基酸、蛋白质、DNA均为手性分子。手性分子的分析对生命起源的探索、药物的鉴别尤为重要。一般而言,手性分子及其对映异构体与圆偏振光发生相互作用时表现出不同的旋向性,因此,利用圆偏振光测试分子的圆形二色性成为鉴别有机分子手性的有效手段。对分子手性机制的探索则需要实现对分子结构进行有效的调控和比较分析,然而,在原子尺度上调控分子结构目前尚未能够有效实现。
利用微纳尺度的胶体颗粒作为超构原子,模拟有机手性分子结构并组装手性超构分子,不仅为深入理解有机分子的手性行为提供了一个可观测、可调控的模型,也为手性材料的设计与应用提供了基础技术支持(见图1a)。然而,如何有效的操控并精确组装不同的胶体颗粒依然存在巨大的技术挑战。虽然DNA纳米技术的发展为手性超构分子的组装提供了一种有效的手段,然而,其分子结构的可重构性有限,并且分子结构需要事先设计,不能提供真正的实时调控。
日前,美国德克萨斯大学奥斯汀分校郑跃兵教授(点击查看介绍)课题组报道了手性超构分子的全光学组装和探测的新技术,并实现了手性超构分子的实时可重构性与手性光学性能的可调制性。相关的工作发表在Materials Today 上。
该研究团队在近年来研制了低功率的热电纳米光镊技术,实现了不同低维材料的无损光学操控与原位光学探测(Nat. Photon., 2018, 12, 195),并基于此开发了胶体材料的光热组装技术(Sci. Adv., 2017, 3, e1700458)。在此项研究中,该研究团队进一步将这项技术应用于手性超构分子的全光学组装中。利用激光操控不同尺寸、不同材料的超构原子,将其组装成具有手性构象的超构分子。通过光场的开关态,实现超构分子的组装与分解。并通过调控超构分子结构,实现对手性光学的实时调控。

图1. 手性超构分子的示意图(a)与光镊组装技术(b)
为了有效提高手性超构分子的光学性能,该研究团队选用了不同尺寸的Au、Ag等离激元纳米颗粒和具有高介电常数的Si纳米颗粒作为超构原子,利用热电纳米光镊技术实现了逐个超构原子的精确组装。如下图所示,该研究团队演示了如何将1个1 μm的聚苯乙烯小球,1个400 nm的Au小球,1个300 nm的Si小球以及1个500 nm的Si小球分别组装为具有对映异构的两种手性超构分子的过程。

通过将超构分子固定于固体衬底上,可以对超构分子的结构进行扫描电镜分析,图2所示为由1个1 μm的聚苯乙烯小球,1个400 nm的Au小球,1个500 nm的Si小球以及1个700 nm的Si小球所组装的手性超构分子的扫描电镜照片。

图2. 手性超构分子的扫描电镜分析
同时,该研究团队还利用圆偏振光激发超构原子的暗场散射光谱,在组装过程中对不同构型的超构分子的圆形二色性进行实现分析。值得一提的是,手性超构分子的分子结构的可重构性与圆形二色性的原位探测为其手性机制的研究提供了新的技术方法。如图3所示,该研究团队演示了将同样的1个1 μm的聚苯乙烯小球,1个400 nm的Au小球,1个500 nm的Si小球以及1个700 nm的Si小球组装成3组不同的对映异构体,其分子结构与圆形二色性的关联性表明,400 nm的Au小球、500 nm的Si小球与1 μm聚苯乙烯小球之间的耦合决定了整个超构分子在850 nm以下的手性,而400 nm的Au小球、700 nm的Si小球与1 μm聚苯乙烯小球之间的耦合则决定了超构分子在850 nm以上波段的手性。
该研究团队认为,手性超构分子的全光学可重构组装不仅为手性材料的内在物理机制研究提供了新的技术手段,该技术的研究也将促进手性光学器件的制备与应用。
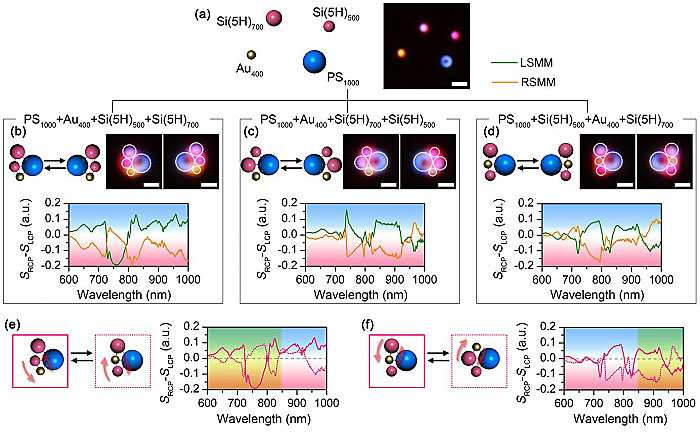
图3. 手性超构分子的可重构性与圆形二色性的原位分析
该论文作者为:Linhan Lin, Sergey Lepeshov, Alex Krasnok, Taizhi Jiang, Xiaolei Peng, Brian A. Korgel, Andrea Alù, Yuebing Zheng
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

All-optical reconfigurable chiral meta-molecules
Mater. Today, 2019, DOI: 10.1016/j.mattod.2019.02.015
导师介绍
郑跃兵
https://www.x-mol.com/university/faculty/38310
课题组链接
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号