“正面硬刚”:陈俊丰团队Science报道不对称亲卤亲核取代反应(SN2X)
单分子亲核取代(SN1)和双分子亲核取代(SN2)是有机化学中的教科书反应(图1A),然而消旋的三级亲电试剂参与的对映选择性亲核取代反应的研究直到近期才崭露头角。其中,SN1反应通常需要能够形成稳定碳阳离子中间体的底物。在这方面,Jacobsen及其同事报道了非杂原子稳定的碳阳离子用于三级乙酸炔丙酯的对映选择性烯丙基化(图1B)。孙建伟课题组报道了邻位酚羟基稳定的碳阳离子与吲哚反应,由此得到消旋的三级烷基醇。SN2反应借助其立体专一性在动力学拆分中具有广泛应用,但很少用于对映选择性合成。相比而言,单分子自由基亲核取代(SRN1)反应对空间影响不敏感,一定程度上可以弥补经典取代反应(SN1及SN2反应)的很多不足,Gregory C. Fu发展的铜催化三级卤代烷烃与胺类底物的不对称自由基取代反应成为这一领域的代表性成果(图1B)。
常规SN2反应的关键特征是亲核试剂从离去基团(X,通常是卤素)背面进攻,会受到空间位阻的影响。相比之下,亲卤亲核取代的SN2X反应鲜有报道,该类反应通过亲核试剂(Nu)从C-X键前方接近,产生碳阴离子和新的亲电中间体(Nu-X),然后碳阴离子取代X产生相应的取代产物。这种途径通常在碳原子中心发生亲核取代困难时进行,为不对称构建空间位阻大的三级或四级立体中心提供了一种有效的方法。
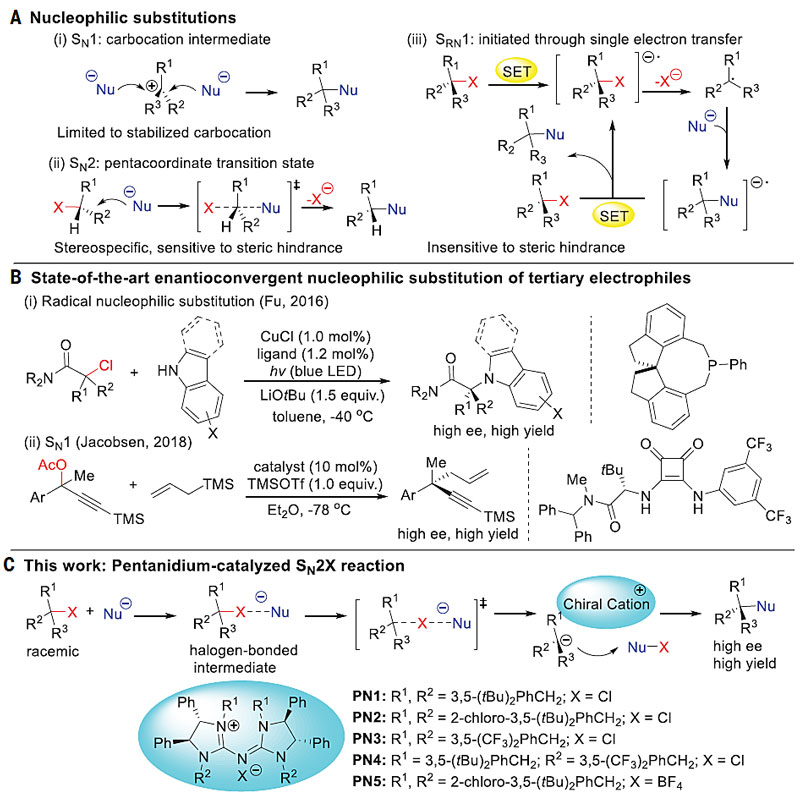
图1. 亲核取代反应。图片来源:Science
近日,新加坡南洋理工大学的陈俊丰(Choon-Hong Tan)教授(点击查看介绍)团队基于前期对卤键的深刻理解,报道了硫代羧酸盐或叠氮化物作为亲核试剂,盘扭五氮胍盐(pentanidium)手性催化剂诱导三级溴化物的对映选择性取代反应。机理实验和计算表明反应中分别经历苯甲酰基亚磺酰溴和BrN3中间体,符合SN2X机制。相关工作发表在Science 上,共同第一作者为Xin Zhang和Jingyun Ren博士。

陈俊丰(Tan Choon-hong)教授。图片来源:南洋理工大学
首先,作者选择三级溴化物1a作为模型底物,在5 mol%的盘扭五氮胍盐作为催化剂时探究各种硫代羧酸盐发生反应的情况(图2A)。他们发现使用噻吩基硫代羧酸钾2b和盘扭五氮胍盐PN4可以得到最佳的结果。在优化的反应条件下,作者考察了底物的适用范围(图2B)。苯基、噻吩基和呋喃基硫代羧酸盐都能以高产率和高对映选择性参与反应得到3a-3c。伯和仲烷基修饰的2-溴-2-氰基乙酸甲酯作为底物可以良好的收率和对映选择性得到产物3d-3h。该反应对于带有烯丙基(3i-3k)和炔丙基(3l)取代基的底物同样有效。对于苄基取代的底物,芳基修饰吸电子和给电子基团对反应均不会造成明显的影响(3m-3q)。
有机叠氮化物在合成化学中具有重要的应用,但手性三级叠氮化物的制备仍然是一个挑战。因此,作者进一步探索了三级溴化物与叠氮化钠的对映选择性取代反应。经过反应条件的优化,作者发现3 mol%的PN5和2.0当量的NaN3在二异丙醚和饱和K2CO3的两相混合介质中-40 ℃低温条件下反应3至4天可顺利实现三级溴化物6a到叠氮化物7a的转化,反应具有良好的收率(86%)和对映选择性(ee 94%)(图2C)。反应缓慢的原因可归因于NaN3在非常低的反应温度下于两相混合溶剂体系中溶解度较低。甲基和苯乙基取代的溴代物参与反应具有良好的效果(7b和7c)。具有庞大取代基的三级溴化物参与反应产率略低(7d-7g),含有烯基和炔基取代基的底物可以良好的收率和对映选择性得到产物7h-7j和7m。环丙基和戊烯基取代的底物用作自由基探针时未形成任何开环或闭环产物,表明自由基物种不太可能参与反应。
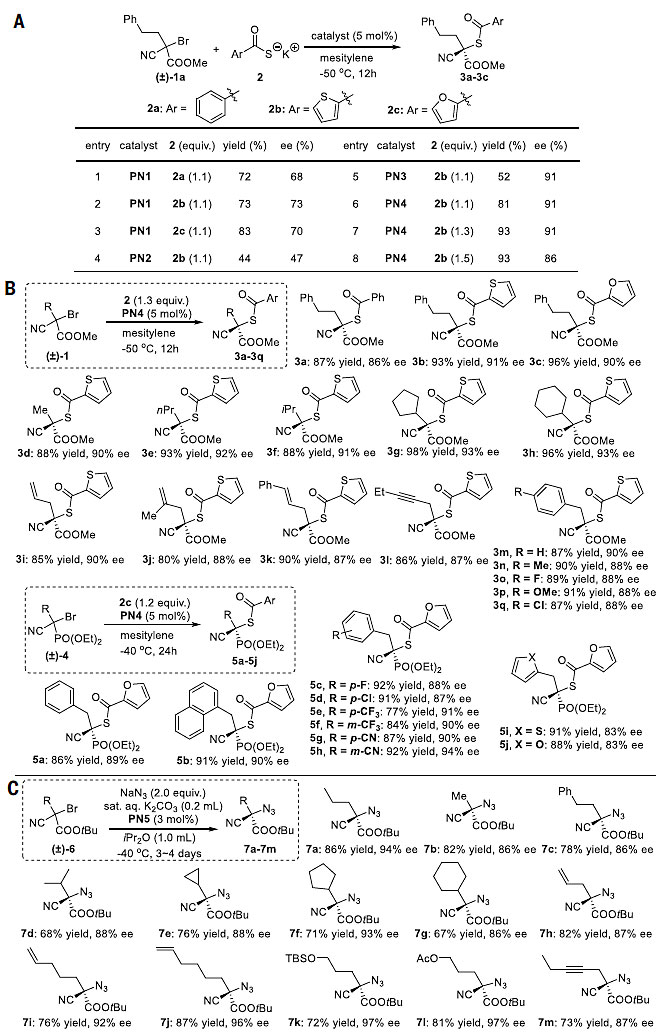
图2. 盘扭五氮胍盐催化的SN2X反应。图片来源:Science
此外,作者对反应的机理进行了系统研究。首先,自由基捕获剂TEMPO、氧化还原捕获剂m-二硝基苯均未显著影响取代反应发生。他们还向三级溴化物1a和噻吩基硫代羧酸钾2b反应的体系中添加质子供体或氢原子供体,氢原子供体不影响反应,但质子供体促进质子化产物1a-H的形成。作者推测如果1a-H是通过碳负离子中间体的质子化产生的,那么在Hammett实验中应该能够观察到该碳负离子的取代基效应。正如作者所推测的,Hammett图表现出正的线性相关性(图3B)。作者还进行了碳阴离子交换实验,以提供碳负离子中间体的实验证据(图3C)。结果表明,1l产生的初始碳负离子从1m-H中攫取质子生成相应的碳负离子。两个碳阴离子与亚磺酰溴反应生成三级硫酯3n和3o的混合物。这些实验结果暗示反应经历了SN2X途径。为了支持SN2X反应的关键特征,即亲核试剂(Nu)对卤素原子(X)进攻产生新的亲电子中间体(Nu-X),作者进一步使用苯甲酰基亚磺酰溴8a和BrN3进行反应,证实了8a和BrN3都是SN2X的合理中间体(图3D)。接下来,作者使用两种对映体富集的三级溴化物1i进行反应,结果发现两种对映体都转化为相同的硫酯对映体,并且回收的1i发生外消旋化(图3E)。据此,作者认为亚磺酰溴和BrN3是通过SN2X机制产生的。作者进一步假设C-Br键断裂步骤是可逆的,由此解释了外消旋化的成因,并提出了SN2X的反应途径和可能的副反应(图3F)。
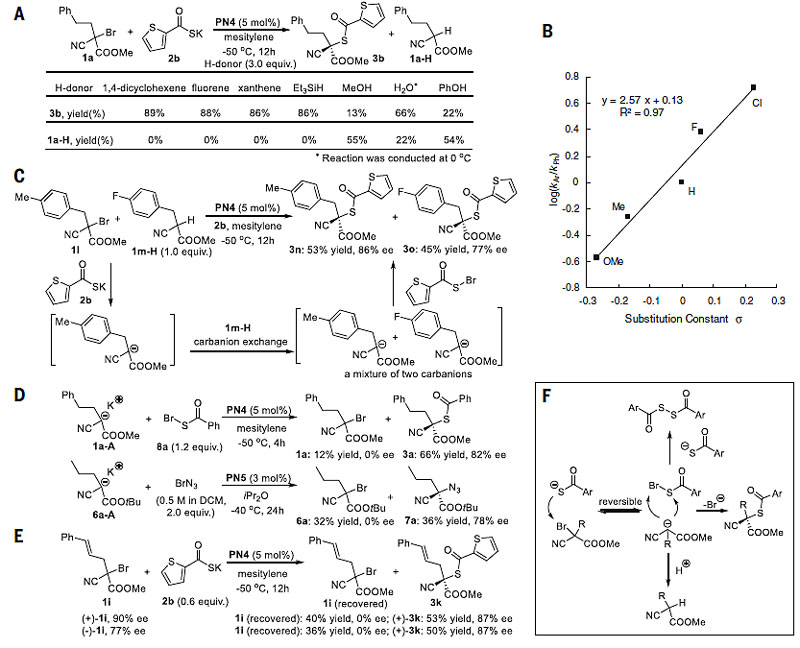
图3. 机理研究。图片来源:Science
最后,作者对3d形成的两种可能途径(SN2或SN2X)进行理论建模,利用DFT计算对SN2X机理提供了更多理论支持(图4)。反应经历SN2途径时会形成TS-A过渡态,能垒较高,而在SN2X途径中存在S-Br卤键相互作用,C-Br键易发生断裂。
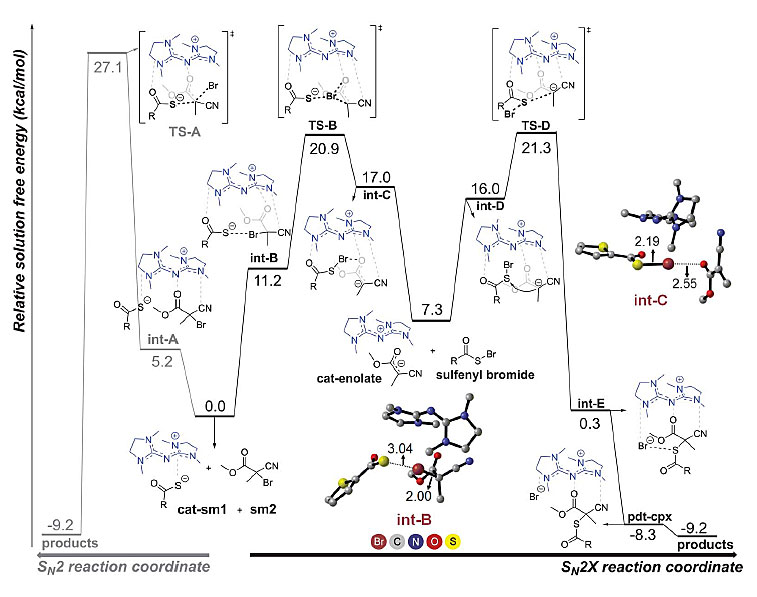
图4. DFT计算。图片来源:Science
结语
SN2X反应途径不会受到空间位阻的影响,意味着以往有机化学中某些难以实现的反应可能通过该途径更有效地进行。尽管卤键的概念已在超分子化学和晶体工程领域得到充分利用,但在合成方法学开发和催化反应设计中的应用仍处于起步阶段。陈俊丰教授课题组基于前期在卤键方面的研究,成功实现了三级溴化物的对映选择性取代反应,并通过实验和理论计算证实反应经历SN2X途径。这一突破性成果无疑为卤键在合成与催化方向的应用探索打开了大门。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

An enantioconvergent halogenophilic nucleophilic substitution (SN2X) reaction
Science, 2019, 363, 400, DOI: 10.1126/science.aau7797
导师介绍
陈俊丰
https://www.x-mol.com/university/faculty/4457
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号