ACS AMI|新型光敏材料促进IPS细胞对药物的通透性
英文原题:Photoactive Oligo(p-phenylene vinylene) Material for Functional Regulation of Induced Pluripotent Stem Cells

通讯作者:陈韵岱*,中国人民解放军总医院;刘礼兵*,中国科学院化学研究所
作者:Yuqi Liu, Liuyang Tian, Yang Li, Yanyan Chen, Yundai Chen*, Libing Liu* and Shu Wang
心血管疾病的发病率目前处于全球增长阶段,且罹患心血管疾病的死亡率远高于癌症和其他疾病,目前心血管疾病的基础和临床研究都有快速的进展,但是由于临床病人心脏组织取材的限制,在很多研究方面仍面临很多瓶颈。多能干细胞诱导分化心肌细胞技术(induced pluripotent stem cell--derived humancardiomyocytes)为心血管疾病的研究提供了技术支持,但是由于细胞膜的选择透过性限制了许多干预药物或者分子进入心肌细胞。
近期,中国科学院化学研究所王树教授,刘礼兵教授课题组和中国人民解放军总医院陈韵岱教授和刘昱圻副教授课题组发现了一种可以辅助增加药物递送进入IPSC细胞内调节心肌细胞功能的光敏材料。研究人员按照5:30:60:3:2的比例混合低聚(对苯乙烯)功能的磷脂,1,2-二油基-sn-甘油-3-磷酸乙醇胺,棕榈酰-2-油基-甘油-3-磷酸胆碱,1,2-二油基-3-三甲氨基丙烷和胆固醇,生成全新的光敏感性聚合物OPFL(图1B-C)。OPFL可以快速地与细胞膜融合,内吞进入细胞,并辅助细胞外的药物或分子进入细胞内。本研究,通过OPFL递送药物进入心肌细胞的作用,实现了环孢素A(线粒体膜通道蛋白选择性抑制剂)进入心肌细胞(图1A)。此外,本研究发现,CsA在OPFL的作用下,可以明显减少心肌细胞中细胞质和线粒体的ROS合成含量(图2),同时减少心肌细胞内胞浆内钙超载,提高线粒体对钙离子调节作用(图3),提高心肌细胞线粒体膜电势(图4),减少心肌细胞的凋亡(图5)。由于,OPFL的特殊的分子结构和功能,使得OPFL不仅仅是一种简单的分子标记探针,更是为药物递送入细胞提供了一种全新的途径。
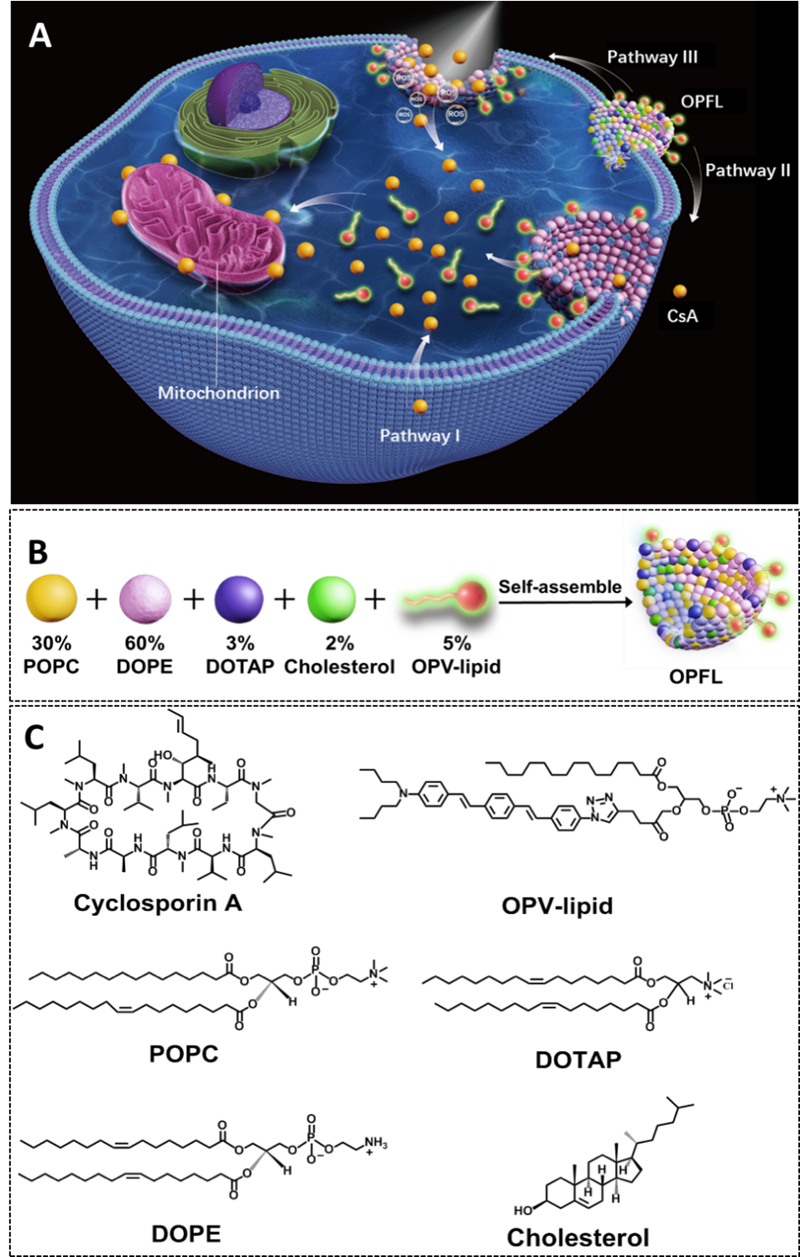
图1. 光敏材料促进药物进入细胞的过程。(A)OPFL与细胞膜融合并辅助环孢素A进心肌细胞途径。(B)OPFL的分子合成比例。(C)OPFL各组分的化学结构式。
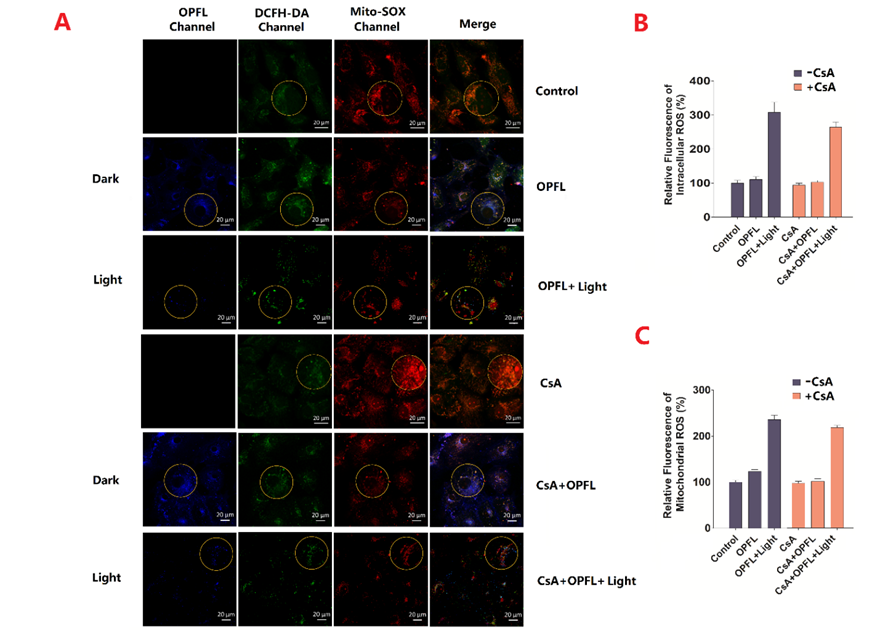
图2. 细胞内ROS的生成。(A)ROS生成的免疫荧光图片,绿色代表细胞质中的ROS,红色代表线粒体中的ROS。(B)光照(+/-)与CSA(+/-)的细胞质中ROS生成含量的对比。(C)光照(+/-)与CSA(+/-)的线粒体中ROS生成含量对比。
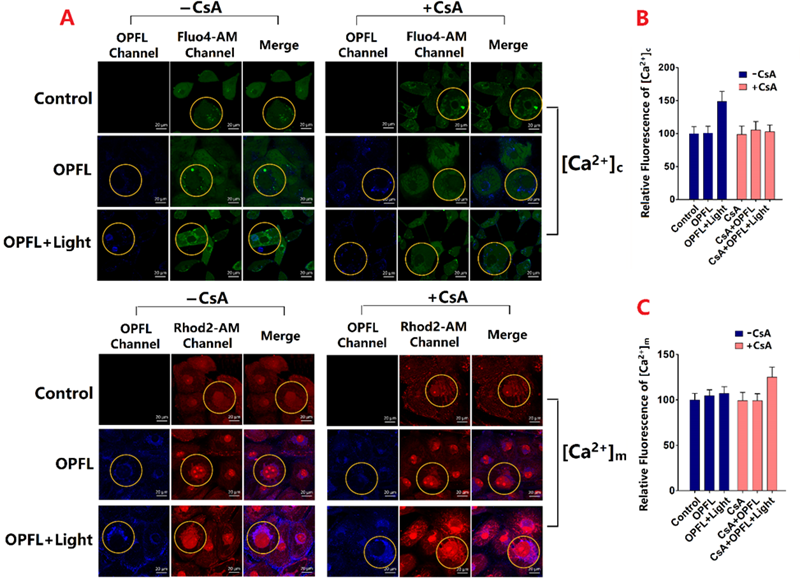
图3. 细胞质和线粒体中Ca2+浓度的变化。(A)Ca2+浓度的图像变化,绿色荧光是细胞质中Ca2+浓度,红色荧光是线粒体Ca2+浓度。(B)光照(+/-)与CSA(+/-)的细胞质中Ca2+浓度对比。(C)光照(+/-)与CSA(+/-)的线粒体中Ca2+浓度对比。
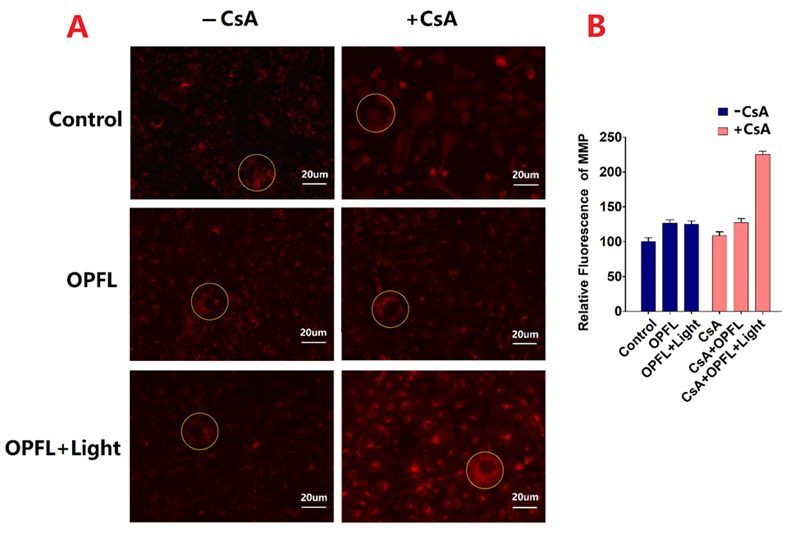
图4. 线粒体膜电位的变化。(A)线粒体膜电位的图像变化。(B)光照(+/-)与CSA(+/-)的线粒体膜电位的改变情况。
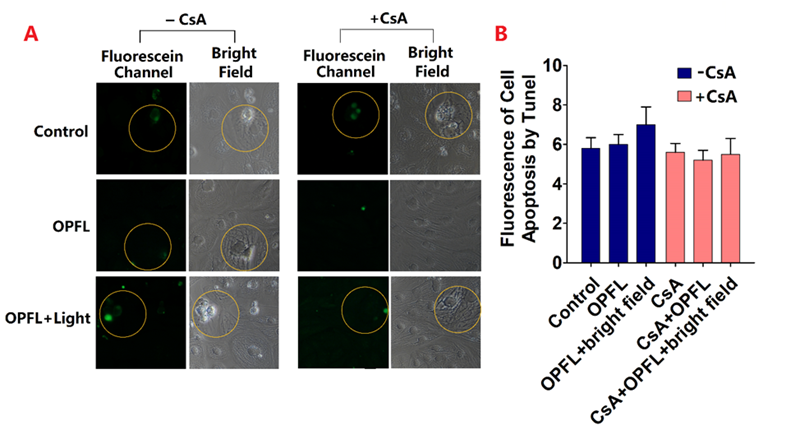
图5. 细胞凋亡情况比较。(A)心肌细胞凋亡的图像变化。(B) 光照(+/-)与CSA(+/-)的细胞凋亡改变情况。
ACS Appl. Mater. Interfaces, 2019, ASAP
Publication Date: December 26, 2019
https://doi.org/10.1021/acsami.9b19331
Copyright © 2019 American Chemical Society
扫描二维码阅读英文原文,或点此查看原文

如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号