烷基草酸酯与烯丙基碳酸酯双重C-O键断裂构建烯丙基化季碳中心
烷烃的烯丙基化反应是一类重要的有机反应,有着广泛的应用价值。同时,含季碳中心化合物的合成在有机化学中具有一定的挑战性,在材料化学和药物分子领域等也有良好的应用前景。
最近,上海大学龚和贵教授(点击查看介绍)课题组开发了廉价金属铁促进的三级烷基草酸酯与烯丙基碳酸酯的还原偶联反应,通过两次C-O键的断裂,成功构建烯丙基化的季碳中心 (如图1所示)。
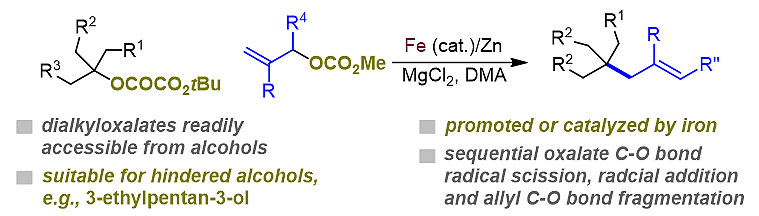
图1. Fe催化的三级烷基草酸酯与烯丙基碳酸酯的还原偶联反应
该方法采用Fe(acac)3为促进剂(不加Fe时,反应产率为~40%),dtBBipy为配体,MgCl2为添加剂,Zn为还原剂,DMA为溶剂 (图2),对于含偕二甲基的季碳中心产物,及含更大位阻的三级烷基均可得到中等到良好的收率 (图2)。同时,该反应对于含环状季碳中心产物及含天然骨架 (如cyclotryptamine及 (+)-cedrol)的烯丙基化产物效率也较好。对于含吸电子或给电子修饰的2-芳基烯丙基酯,反应也都能给出较好的产率。然而在标准条件下,没有如何取代基团的简单烯丙基碳酸酯的偶联产率<10%,进一步优化后发现采用烯丙基醋酸酯为底物,FePc为催化剂,tBu-Ter-Pyridine为配体,烯丙基化产率可以达到49%(图2最后的例子)。

图2. 反应底物的拓展
此外,该方法还适用于三级烷基草酸酯与烯丙基碳酸酯及丙烯酸酯的三组份反应。采用5 mol%的催化剂,三组份反应的产率一般在42-56%范围内。有趣的是炔丙基酯也能参与该反应,并给出27%收率的双烯产物 (图3)。

图3. 三组份反应及底物拓展
上述三组分反应从侧面说明该反应可能是自由基串联反应机理。这一假设可以通过三级草酸酯的分子内自由基关环/烯丙基化实验得到验证。如图4所示,相应的关环/烯丙基化产物的产率在39-61%的范围。对烯丙基碳酸酯末端烯氢进行氘代标记,偶联反应只观测到三级烷基自由基加成到烯烃末端的产物,说明反应过程中没有π-allyl-Fe中间体的参与。因此,该反应中的烯丙基C-O键断裂可能是自由基反应中的一个较新的模式。我们推测反应的机理中MgCl2与烯丙基碳酸酯的络合可能在烯丙基C-O键断裂中起到了关键作用,Fe离子起到了与Mg离子相似的作用,促进了反应的进行。具体的反应机理需要更进一步的研究 (图5)。

图4. 自由基关环/烯丙基化反应
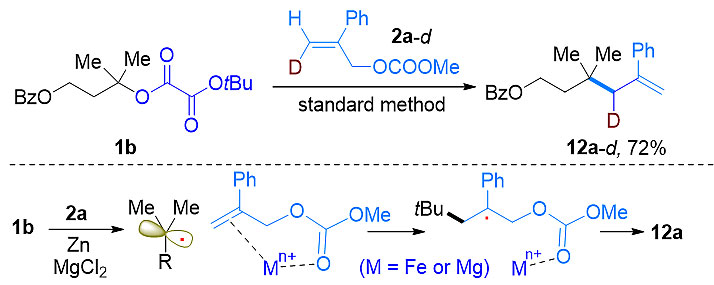
图5. 反应机理假定
总之,该方法为构建含全C(sp3)的季碳中心提供了一条新的合成途径。反应过程中MgCl2起到了活化草酸酯及烯丙基碳酸酯的双重作用,从而使该反应可以采用一种较新的自由基C-O/C-O键断裂方式生成烯丙基化的季碳中心产物。
本研究工作第一作者是上海大学材料学院的博士生陈海峰。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Formation of allylated quaternary carbon centers via C–O/C–O bond fragmentation of oxalates and allyl carbonates.
Haifeng Chen, Yang Ye, Weiqi Tong, Jianhui Fang, Hegui Gong
Chem. Commun., 2020, 56, 454-457. DOI: 10.1039/c9cc07072a
导师介绍
龚和贵
https://www.x-mol.com/university/faculty/12427
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号