人造红细胞用于乏氧肿瘤的光动力学治疗
肿瘤部位极度乏氧的微环境是阻碍肿瘤治疗的主要障碍之一。红细胞是血液中最多的血细胞,负责机体内营养物质和氧气的运输,维持机体的正常运转。有没有可能利用红细胞携带氧气的功能来解决肿瘤的乏氧问题,从而提高肿瘤治疗效果呢?近日,武汉大学的张先正教授(点击查看介绍)和冯俊教授(点击查看介绍)团队制备了一种具有攻击性的人造红细胞(AmmRBC),克服肿瘤组织乏氧对光动力学治疗(PDT)的抗性。
PDT具有可控性好、副作用小等优点,被认为是治疗肿瘤的有效手段。氧气是光激活产生活性氧(ROS)引发细胞死亡PDT过程中不可或缺的。但是,肿瘤组织的乏氧特征严重抑制了PDT的治疗效果。而且,PDT过程中快速耗氧会引起多米诺效应,进一步抑制光动力学治疗。对此,国内外研究人员通过肿瘤定向携氧和瘤内产氧等策略来提高肿瘤中的氧含量,但这些策略都需要复杂的化学合成和繁琐的制备过程;而且还存在一些较难克服的问题,包括氧气供应不足和所携带组分(如氧气和用于产生氧气的过氧化氢等)的快速泄漏。
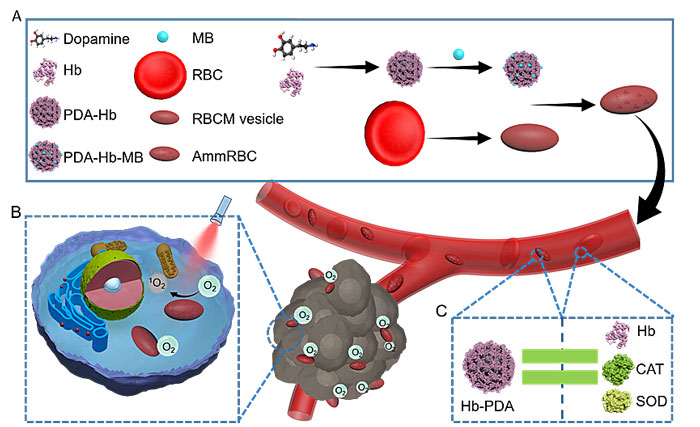
武汉大学的研究团队报导的攻击性人造红细胞较好地解决了上述问题。红细胞富含血红蛋白(每一个红细胞包含大约3.7亿个血红蛋白分子),而血红蛋白是红细胞高效运载氧气的根源。血红蛋白自身在循环过程中和肿瘤内增高的氧化环境中容易氧化,导致其失去携氧能力,同时产生有毒物质,比如高价铁血红蛋白。为了抵抗对血红蛋白的氧化损伤,红细胞拥有包含特殊酶在内的天然抗氧化系统,包括超氧歧化酶、过氧化氢酶等。受红细胞的生物特性启发,该研究模拟设计了一种人造红细胞来实现自供氧的肿瘤光动力学治疗。具体而言,血红蛋白、聚多巴胺(PDA)和光敏剂封装在重组红细胞膜囊泡中制备出AmmRBC。其中,血红蛋白作为氧气载体携氧;PDA模拟天然红细胞中抗氧化酶的功能防止血红蛋白氧化;同时PDA有很多芳香环,为光敏剂或化疗药物提供了吸附位点。外层的红细胞膜囊泡则可以提高生物相容性和实现体内长循环。实验表明,AmmRBC能够在肿瘤部位富集,改善肿瘤部位乏氧状况,提高PDT效果,从而杀死肿瘤。由于PDA能吸附多种治疗药物,mmRBC也可以进一步作为氧气自供的通用平台来敏化传统肿瘤治疗中由于乏氧造成的治疗抗性。
这一成果近期发表在Advanced Materials 上,文章的第一作者是武汉大学的博士研究生刘文龙和刘涛。
该论文作者为:Wen-Long Liu, Tao Liu, Mei-Zhen Zou, Wu-Yang Yu, Chu-Xin Li, Zu-Yang He, Ming-Kang Zhang, Miao-Deng Liu, Zi-Hao Li, Jun Feng, and Xian-Zheng Zhang
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Aggressive Man-Made Red Blood Cells for Hypoxia-Resistant Photodynamic Therapy
Adv. Mater., 2018, DOI: 10.1002/adma.201802006
导师介绍
张先正
http://www.x-mol.com/university/faculty/13628
冯俊
http://www.x-mol.com/university/faculty/13630
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
林文斌团队:光动力学敏化肿瘤环境,唤醒免疫卫士抗癌 2017-01-31
-
基于硫化氢特异性激活纳米MOF光敏剂调控活性氧释放的光动力学治疗癌症 2018-02-08
-
苯并卟啉基金属有机框架材料用于肿瘤转移的治疗 2018-05-31
-
近红外光/H2O2触发的智能纳米器件用于乏氧肿瘤的高效及选择性光动力学及光热协同治疗 2016-08-02
-
Red blood cell membrane nanoparticles for tumor phototherapyColloids and Surfaces B: Biointerfaces (IF 5.4) Pub Date : 2022-10-08 ,DOI:10.1016/j.colsurfb.2022.112895Bing-De Zheng, Mei-tian Xiao


































 京公网安备 11010802027423号
京公网安备 11010802027423号