化学“神技术”综述(六):晶体海绵法,不需要长单晶的单晶结构解析
如果说化学是21世纪的“中心学科”,那么结构表征毋庸置疑是化学研究的核心问题。在众多的化学表征手段中,最直观最准确的分析方法无疑是——单晶结构解析(Single X-ray crystallographic analysis)。生长出质量合适的单晶是该分析方法最大的瓶颈,相信大多数的化学、生物研究者都经历过长单晶的痛苦,问题可以说是层出不穷,比如:液体化合物根本就无法结晶;核磁、质谱等等分析手段无法确定化合物的取代基团的位置,只有寄希望于单晶结构解析,可是却迟迟拿不到单晶;合成的样品量太少(< 1 mg),基本没有希望长出好的单晶。幸亏,化学家们发明了“晶体海绵法”(crystalline sponge method),可以解决这些问题,突破单晶结构解析的瓶颈。下面就给大家介绍一下“晶体海绵法”的前世今生。

(一) 起源:溶液相主化学的可视化
化学中的一个重要的挑战就是可以观测到分子运动和分子反应过程。其中单晶结构快照(X-ray snapshot observation)观测提供了最为直观的证据。而要实现这个过程,就需要有合适的、刚性的载体,且该载体可以在化学反应前后保持其单晶性。金属有机框架(Metal-organic Frameworks,MOFs)恰恰是这样一个合适的材料。2009年,日本东京大学的Makoto Fujita教授团队报导了利用MOFs作为载体,实现了对于亚胺合成反应的可视化观测(Nature, 461, 633-635, 2009)。
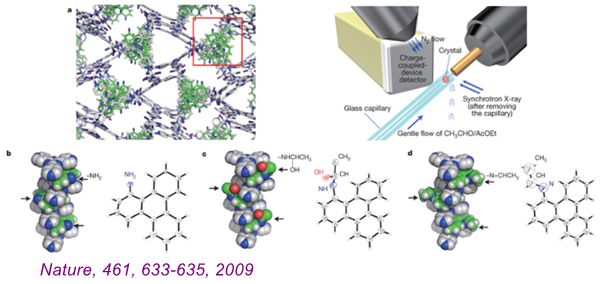
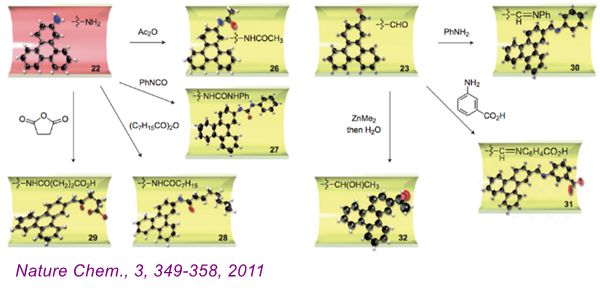
当初始的芳香胺MOFs晶体(上图b)和乙醛反应时,通过控制反应温度(215K)和反应时间(10min)(实验装置如上图a右) 不稳定的半缩醛胺中间产物(在溶液中难以检测) 被稳定在MOFs框架中 (上图c)。当升高温度,半缩醛胺将进行脱水反应生成亚胺(上图d)。通过在线的单晶结构快照,整个单晶到单晶的反应过程被直观的纪录下来。除此之外,Fujita 团队还利用此方法观察到了酰化、Huisgen 环加成、立体选择性D-A反应等等(见下图)(详情见综述文章Nature Chem., 3, 349-358, 2011)。
多年的溶液相化学的可视化的研究奠定了“晶体海绵法”的基础,揭示了“晶体海绵法”的可行性。首先,分子在多孔的MOFs材料中还是保留着其溶液相的特性;其次,外来客体分子可以长程有序的排列在MOFs材料的孔道内。(注:长程有序是保证单晶结构解析的必要条件,无序的分子排列无法得到好的晶体数据和结构解析结果)
(二) 晶体海绵法的诞生
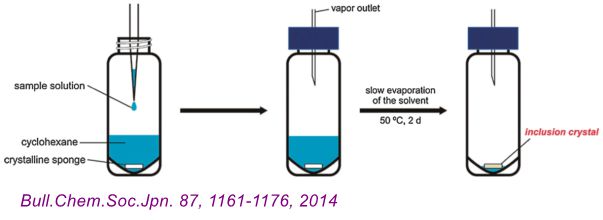
以多年的溶液相化学的可视化研究为基础,Fujita教授团队于2013年报导了“晶体海绵法” (Nature, 495, 461-466, 2013)。其方法包括以下几个步骤:1)制备晶体海绵;2)目标客体包裹;3)客体包裹晶体的单晶结构解析。(如上图)
“晶体海绵法”最大的突破在于以下几点:1)不需要任何结晶过程,随着样品溶剂的挥发,目标分子会自动渗透进入晶体海绵内部,并长程有序排列在晶体海绵的孔洞里 (晶体海绵就好比已经建好的房子,目标分子就好比将要入住的住户,每一个住户都按照事先安排好位置入住每一间房间,从而实现长程有序);2)可以实现纳克级化合物的晶体结构分析。理论上,一颗 (80 × 80 × 80 μm3)的晶体海绵就可以实现26纳克的目标分子的结构解析;3)可以与高效液相色谱(HPLC)联用,实现对于少量混合产物的直接结构分析;4)可以确定分子的绝对构型(如上图所示,a. 目标分子在晶体海绵中的排列;b. 目标分子的晶体结构)。
(三) 晶体海绵法的拓展
随着“晶体海绵法”的提出,Fujita研究组开始着力于规范化和流程化其实验操作步骤(Nat. Protoc., 9, 246–252, 2014),让“晶体海绵法”可以更简单可行应用于化学结构测定的各个领域。下面给大家介绍“晶体海绵法”最近的应用实例和改进。
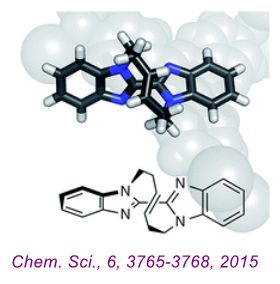
从中心手性到轴手性和面手性: 在之前的文章中(Nature, 495, 461-466, 2013),“晶体海绵法”已经可以用于确定分子的绝对构型(主要为中心手性),除此之外,分子还有其他的手性,包括轴手性,面手性以及螺旋手性等。最近Fujita研究组报导了轴手性和面手性分子的绝对构型的测定,进一步拓展了“晶体海绵法”的应用范围(Chem. Sci., 6, 3765-3768, 2015)。该研究揭示了晶体海绵结构的柔韧性,通过包裹手性目标分子,其可以实现从非手性空间群向手性空间群的转变。
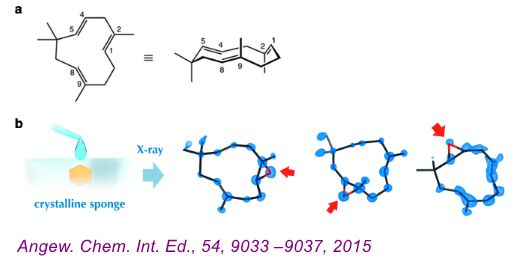
确定化学反应位点:如何确定具有多个相似的反应活性位点的分子在发生化学反应时的准确反应位置,往往是十分困难的。(比如蛇麻烯a-Humulene的氧化,下图a,三个烯烃的都可以为氧化的反应位点,且每个位点都可以有不同的立体化学)。利用“晶体海绵法”独特优点,Fujita研究组成功的确定了在不同氧化条件下,蛇麻烯的氧化位点以及空间立体化学(Angew. Chem. Int. Ed., 54, 9033 –9037, 2015)。
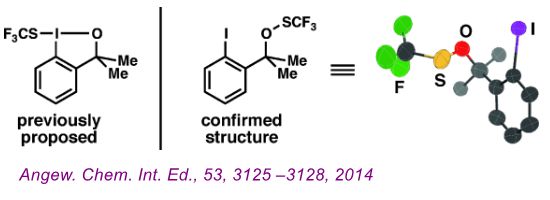
应用于有机合成研究:2013年,Shen教授研究团队分离了Trifluoromethylthiolation反应中重要的无色油状中间体,通过核磁、元素分析等表征手段(无单晶证据),其研究团队认定这是一个新的超价碘试剂(如下图左)。2014年MIT的S. L. Buchwald教授团队通过核磁等研究发现该试剂可能存在开环形式,结合“晶体海绵法”其研究团队得到了该中间试剂的晶体结构,证实了其开环形式的存在(如下图右)(Angew. Chem. Int. Ed., 53, 3125 –3128, 2014)。
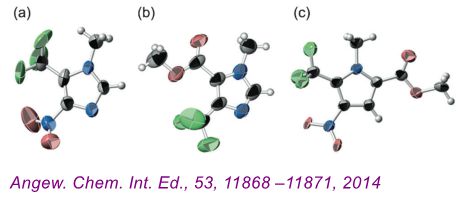
除此之外,同年美国Scripps研究所的Phli S. Baran教授研究团队报导了运用电化学反应实现杂环芳烃的C-H功能化(Angew. Chem. Int. Ed., 53, 11868 –11871, 2014)。其中有几例产物无法确定三氟甲基化位点。通过运用“晶体海绵法”就直观确定了仅仅2mg产物的反应位点(如下图)。
以上的例子表明,“晶体海绵法”可以应用于有机合成的各个方面,对于确定复杂的中间产物和最终产物的立体化学的结构有着十分显著的帮助。今后可以预期越来越多研究组将利用“晶体海绵法”解决其研究中遇到的分子结构表征问题。
其他研究组的改进和贡献:在“晶体海绵法”发表之后,哈佛医学院的Jon Clardy教授团队对其进行了一系列的改进。其研究表明,当使用三氯甲烷取代硝基苯为生长溶剂,可以不需要溶剂交换的步骤,这样使得晶体海绵的制备时间从2个礼拜缩短到仅仅需要3天。除此之外,其研究团队还从晶体学家的角度规范化了了“晶体海绵法”操作流程,包括晶体的生长、挑选,数据的收集、处理和结构的解析流程(Acta. Cryst., A71, 46–58, 2015)。在接下来的研究中,Clardy研究团队发现金属终端配体的不同对于“晶体海绵法”的有着显著的影响。当用相对较轻的终端配体氯或者溴取代较重的碘之后,晶体海绵的框架结构的衍射强度有所降低,但是其客体的电子衍射的可靠性相对而言却进一步提高了。虽然这样的变动,需要延长晶体数据收集的时间和X-ray射线的衍射强度,但是由于晶体海绵的框架结构对于客体分子电子衍射的影响减小,其数据结构的可靠性和质量得到一定提高。此研究对于今后的晶体海绵的开发提供了一定的指导性意见(Chem. Commun., 51, 11252 –11255, 2015)。
(四) 晶体海绵法的局限和展望
由于“晶体海绵法”主要采用ZnI2-TPT的金属有机框架(结构如下图),其局限如下:1)孔洞的大小决定了目标分子的大小,超过孔洞大小的目标分子是无法进入晶体海绵中,从而也无法利用“晶体海绵法”;2)孔洞的环境决定了目标分子的特性,亲水性分子难以进入疏水性的孔洞,所以迄今为止,“晶体海绵法”主要应用于疏水性分子结构的测定;3)晶体海绵的稳定性决定了目标分子的溶液特性,目前仅仅少量的溶剂可供选择,主要为环己烷。对于在环己烷中溶解度差的分子,“晶体海绵法”的成功的报导还较少。
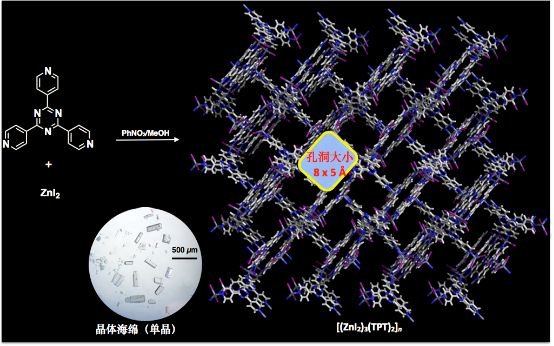
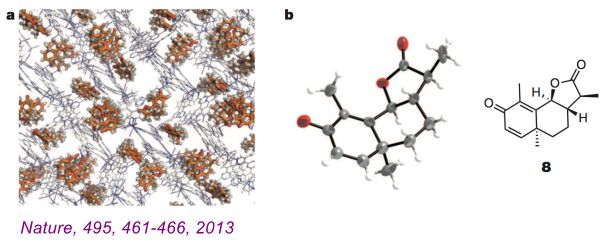
但是,“晶体海绵法”有着不可限量的前景,首先,金属有机框架具有丰富结构数据库,可以预想今后可以从已有的结构中发现新的晶体海绵(下图为一例最新报导的晶体海绵),也可以重新设计合成特异性识别某类目标分子的晶体海绵(比如,氨基酸晶体海绵、糖晶体海绵等等);其次,合成具有超大的孔洞的晶体海绵将有助于解决生物大分子的晶体结构解析(如果这个能够实现,也许“晶体海绵法”也有机会问鼎诺贝尔奖);再次,对于药物研发过程的中间分子的结构测定将是极大的帮助。
(本文由 fukurou 供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!









































 京公网安备 11010802027423号
京公网安备 11010802027423号