尹航课题组发现新型NF-κB小分子抑制剂
细胞转录因子蛋白家族(NF-κB)在细胞免疫、炎症、细胞存活中都扮演着关键作用,开发NF-κB抑制剂对研究其生物学功能和发展抗炎、抗癌药物有重要意义。很多上游免疫蛋白可以激活NF-κB,例如Toll样受体(TLRs)、肿瘤坏死因子受体(TNFR)、白介素-1受体(IL-1R)、T细胞受体(TCR)和B细胞受体(BCR),其中TLRs是研究得比较透彻的一类免疫受体。TLRs蛋白家族会识别不同病原体,而激活下游的NF-κB信号,如TLR4识别LPS、TLR7识别单链RNA等。清华大学尹航教授(点击查看介绍)课题组在TLRs领域有多年研究基础,发表了一系列TLRs家族的小分子免疫调节剂。
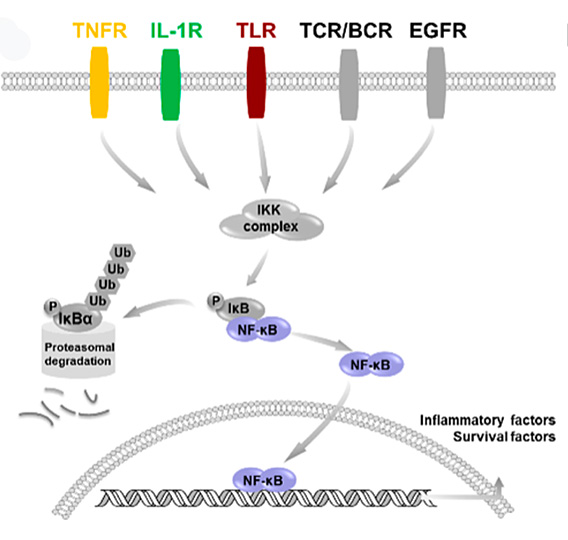
NF-κB的上游信号通路。图片来源:J. Med. Chem.
最近,尹航课题组利用已建立的筛选平台,在过表达TLR7的HEK293细胞中(简称HEK7)通过高通量筛选方法发现了两个苗头化合物,这两个分子都有比较独特的酰肼结构。
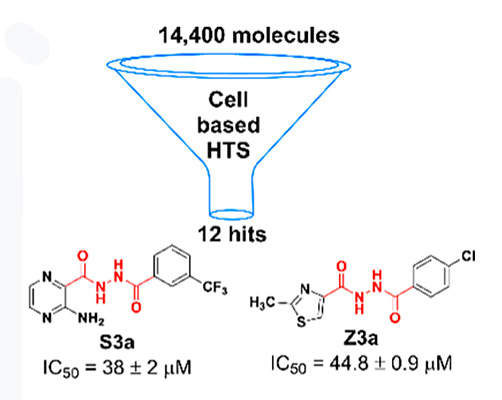
苗头化合物结构式。图片来源:J. Med. Chem.
通过在多种过表达TLRs的HEK293细胞中测试,苗头化合物均表现出一定的抑制作用,因此研究人员认为苗头化合物的靶点不是TLRs,而是更下游的蛋白。
在结构改造环节,研究人员保留了共有的酰肼结构,而重点研究两侧芳香基团的构效关系。实验发现分子抑制活性对芳香基团的改变比较敏感,最终确定了2-吡啶取代基和2,4-二氯苯基噻唑取代基作为活性最好的分子(Z9j),其IC50为0.26 μM,并且在20 μM内没有表现出明显的细胞毒性。

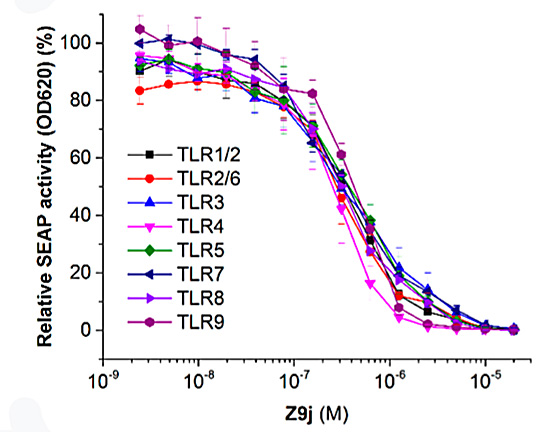
Z9j在不同TLRs中的活性测试。图片来源:J. Med. Chem.
接下来,研究人员重点证明了Z9j抑制活性的分子机制。特异性实验表明Z9j对所有TLRs激活的抑制能力相同,说明其真实靶点很可能是最下游的NF-κB。研究人员还用TNF-α、IL-1β、PMA激活HEK-Blue Null细胞(不表达TLRs,但表达下游的信号通路),Z9j可以成功将其抑制,也佐证了这一观点。
在WT实验中,Z9j能够下调TLRs到NF-κB之间的IKKαβ、IkBα、Akt473、PI3K、p38、p-ERK、Src和Syk的磷酸化。并且能够抑制Src酶的活性。
最后研究人员在细胞层面验证了Z9j的抗炎和抗肿瘤活性。LPS激活Raw264.7细胞是常用的炎症模型。Z9j能够有效抑制TNF-α和NO的分泌(均是炎症信号)。抗肿瘤实验中,研究人员将不同浓度的Z9j与HeLa细胞共培养,5 μM以上既能观察到明显的杀伤作用,40 μM可以杀死约80%的癌细胞。流式细胞术也表明Z9j能够显著增加HeLa细胞晚凋阶段(Q2区域)的比例。

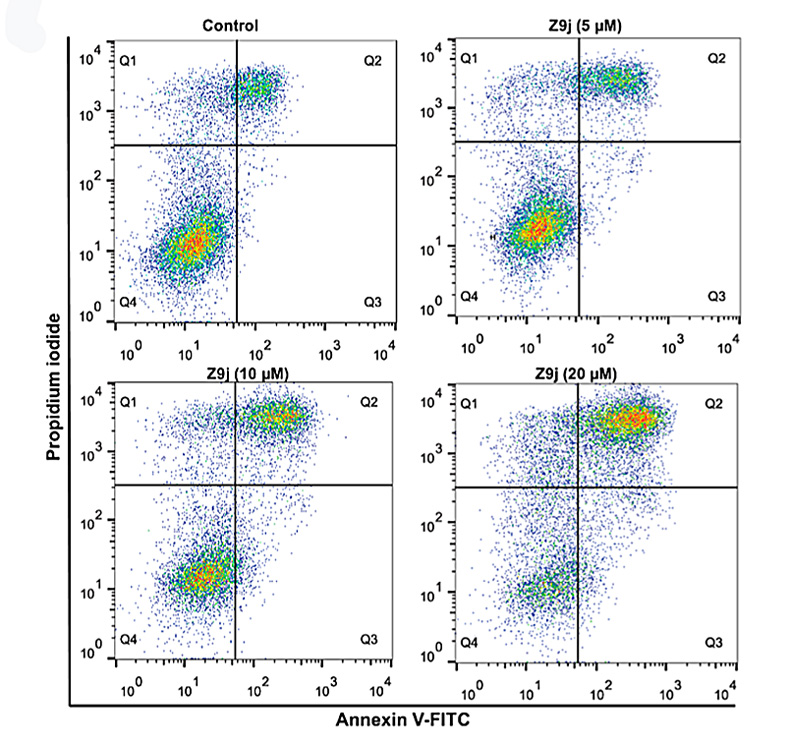
Z9j的抗肿瘤活性。图片来源:J. Med. Chem.
尹航教授课题组通过高通量筛选和构效关系研究将苗头化合物的活性提高了约170倍,并验证了其NF-κB的抑制活性和抗炎抗肿瘤活性。这一方面丰富了研究NF-κB通路分子工具,另一方面提供了一系列有潜力的前药物分子。
(本文作者:颜磊,清华大学基础分子科学中心博士生)
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Discovery of Novel Small-Molecule Inhibitors of NF-κB Signaling with Antiinflammatory and Anticancer Properties
Lei Zhang, Lei Shi, Shafer Myers Soars, Joshua Kamps, Hang Yin
J. Med. Chem., 2018, 61, 5881−5899, DOI: 10.1021/acs.jmedchem.7b01557
导师介绍
尹航
http://www.x-mol.com/university/faculty/46697
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号