新型铜催化环丙醇开环反应
由于其内在的环张力和通过Kulinkovich反应或者Simmons-Smith反应的便捷合成,环丙醇已经成为一种广泛应用于复杂功能分子合成中的起始物或者中间体,一系列环丙醇开环或者扩环的反应也被研发出来。美国普渡大学化学系和癌症研发中心的代明骥(点击查看介绍)课题组最近报道了一系列环丙醇开环偶联反应来促进不同β-取代的酮类化合物的高效简洁合成,其中包括β-CF3、SCF3、CF2R、NR1R2以及含氮杂环取代的酮类化合物。他们还发展了钯催化的羟基取代的环丙醇羰基螺环内酯化反应来快速合成各类螺环内酯,包括复杂天然产物。

近日,该课题组进一步报道了一类新型铜催化环丙醇开环反应并提出新颖的反应机理,此反应可以简洁高效地合成δ-二酮酯和γ-丁内酯,并同时分别快速构建四级碳,在天然产物全合成和药物化学中有潜在的应用。采用方便易得的环丙醇与商业可得的α-溴代酯作为底物,作者发展了两种互补的铜催化剂的反应条件来分别成δ-二酮酯和γ-丁内酯。在CuCl催化的条件下,含有四级碳的δ-二酮酯是主要产物;在Cu(OTf)2催化的条件下,含有四级碳的γ-丁内酯为主要产物;两个反应都具有广泛的底物适用性以及温和的反应条件。
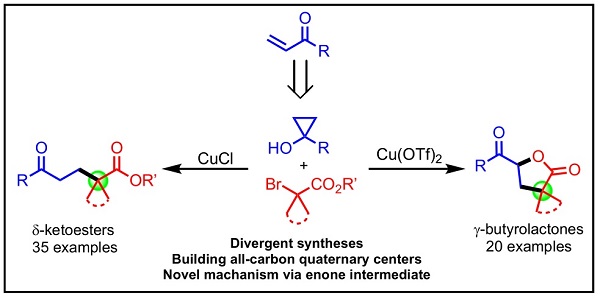
此外,作者还对反应的机理进行了进一步的研究。在环丙醇开环反应中,α,β-不饱和酮是大家普遍认为的副产物之一,经过对一系列不同反应条件和反应底物的详细探索,作者发现α,β-不饱和酮的生成是γ-丁内酯合成途径中的关键中间体。作者还发现碘化钾的使用在α,β-不饱和酮的生成中扮演着重要的作用,环丙醇首先通过碘代开环转化成β-碘代酮,后者通过β-消除反应而生成α,β-不饱和酮。新生成的α,β-不饱和酮再通过分子间的自由基加成和分子内的自由基成环反应等一系列反应过程,可以方便高效地合成γ-丁内酯。
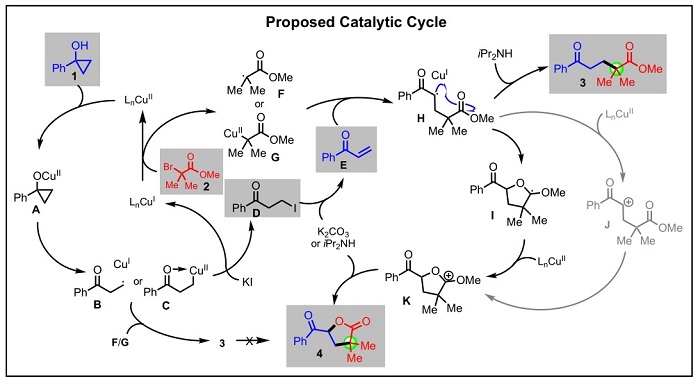
这一成果近期发表在ACS Catalysis 杂志上,文章的共同第一作者是叶智识(Zhishi Ye)博士和博士研究生蔡鑫培(Xinpei Cai)。
该论文作者为:Zhishi Ye , Xinpei Cai, Jiawei Li, Mingji Dai
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Catalytic Cyclopropanol Ring Opening for Divergent Syntheses of γ-Butyrolactones and δ-Ketoesters Containing All-Carbon Quaternary Centers
ACS Catal., 2018, 8, 5907-5914, DOI: 10.1021/acscatal.8b00711
代明骥博士简介

代明骥,四川彭州人,美国普渡大学化学系和癌症研究中心副教授。 2009年于美国纽约哥伦比亚大学取得博士学位,2009年至2012年在美国哈佛大学和Broad研究所从事博士后研究,2012年8月起就职于普渡大学。
研究领域主要包括发展高效新颖的合成方法和策略来对具有复杂结构和显著生物活性的天然产物进行全合成、药物化学和化学生物学研究。在相关领域发表SCI论文50余篇,获授权美国发明专利4项。曾获Amgen Young Investigators'Award, Eli Lilly Grantees Award, 2017 CAPA Distinguished Junior Faculty Award, 2015 Organic Letters Outstanding Author of the Year Lectureship Award, NSF CAREER Award, etc.
http://www.x-mol.com/university/faculty/123
http://www.chem.purdue.edu/dai/
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
碳氢键活化反应中的新偶联组分:环丙醇 2016-03-18
-
环丙醇与重氮化合物的开环偶联反应 2017-07-18
-
铜催化环丙醇的开环三氟甲基及硫三氟甲基化反应 2015-06-01
-
铜催化环丙醇的开环亲电氨化反应 2015-06-10
































 京公网安备 11010802027423号
京公网安备 11010802027423号