发夹型DNA探针用于监测流体剪切力促进细胞的内吞过程
在生命体内,细胞通常处于复杂的微环境中,多种生理条件及相互作用对于维持细胞的正常行为和功能具有重要意义。除了多种化学或生物学因素,细胞也通常处于一个力学微环境中。多种力学作用,如流体剪切力、压力、基质张力和基质硬度等,在细胞的多个生理学过程中具有重要影响,而非正常的细胞力学微环境或细胞力学信号转导则会导致多种疾病的发生。
流体剪切力是细胞力学微环境中一种重要的机械力,它通常由血液或组织间液流动产生,并普遍存在于生命体内。流体剪切力能够影响多个细胞生物学过程,包括细胞自噬、细胞粘附、微绒毛形成等。细胞内吞作为细胞通过质膜的变形运动将细胞外物质通过主动运输的形式转运入细胞内的过程,是真核细胞调节营养物吸收、信号转导和质膜更新的重要方式。目前已有一些研究工作表明,流体剪切力能调控细胞的内吞过程。然而这些方法一般局限于某种目标配体或蛋白以及相应的某类细胞,并且无法实现流体剪切力作用下细胞响应的动态监测。
最近,清华大学的林金明(点击查看介绍)团队在微流控芯片上建立了细胞流动培养平台,并利用标记于细胞表面的发夹型DNA探针,实现了对流体剪切力作用下细胞内吞过程的原位、动态监测。细胞在微流控芯片平台上可实现流动培养,并通过流速的精确控制实时调节细胞感应的流体剪切力大小。发夹型DNA探针两端分别标记荧光染料Cy3和淬灭分子BHQ-2,并以无差别的方式标记于细胞膜表面的蛋白上。初始状态细胞膜上探针荧光淬灭,当细胞进行内吞时,DNA探针会随着细胞膜的内陷和内吞小泡的形成进入细胞。以往的研究工作表明,花青染料(如Cy3等)标记的DNA分子进入细胞后会选择性富集于线粒体上,并打开发夹结构,实现荧光恢复。因此,人们可通过实时观察细胞内的荧光变化,实现对细胞膜表面蛋白内吞过程的监测。该平台可用于系统性地研究流体剪切力作用下不同细胞对于多种蛋白内吞过程的影响。
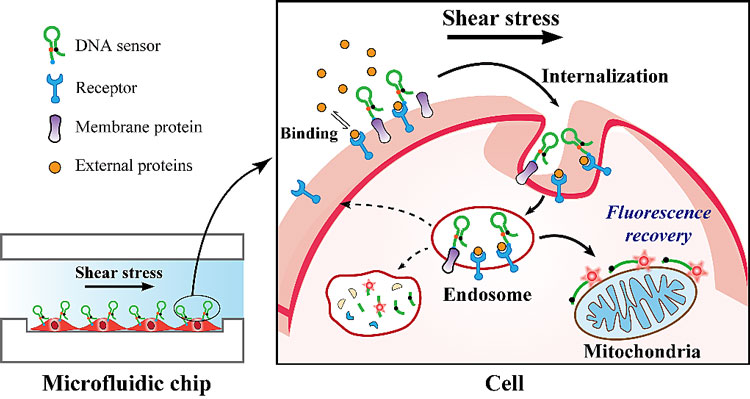
研究发现,在外加蛋白的存在下,流体剪切力能够显著增强细胞内的红色荧光信号。基于荧光共定位实验,他们可确定荧光主要分布于线粒体上。该结果表明,流体剪切力能增强细胞的内吞作用,从而使DNA探针随着细胞表面蛋白受体进入细胞内,进而富集于线粒体上,并实现荧光恢复,该增强作用与剪切力大小密切相关。通过研究流体剪切力对于多种蛋白内吞过程的影响,他们发现该增强过程与蛋白的内吞途径密切相关:流体剪切力显著增强了陷窝蛋白(Caveolae)依赖的内吞途径,而对于网格蛋白(Clathrin)依赖的内吞途径则影响较小。该平台不仅为细胞力学微环境和力转导的研究提供了新的手段,也为细胞内吞等重要生物学过程的研究提供了新的思路。
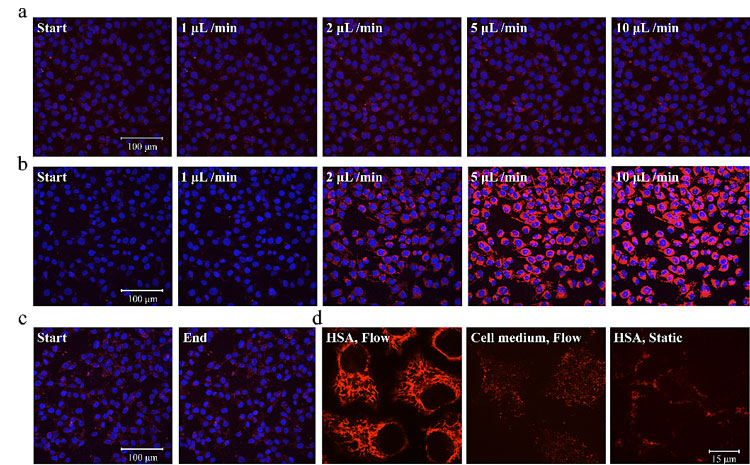
这一成果近期发表在Analytical Chemistry 上。文章的共同第一作者是清华大学的博士研究生何子怡和张婉玲,上述研究得到国家自然科学基金的资助。
该论文作者为:Ziyi He, Wanling Zhang, Sifeng Mao, Nan Li, Haifang Li and Jin-Ming Lin
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Shear Stress-Enhanced Internalization of Cell Membrane Proteins Indicated by a Hairpin-Type DNA Probe
Anal. Chem., 2018, 90, 5540, DOI: 10.1021/acs.analchem.8b00755
导师介绍
林金明
http://www.x-mol.com/university/faculty/12012
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号