铜催化炔丙基磺酸酯的高立体专一性三氟甲基化和二烷基化反应
基于氟原子的特殊性,向分子中引入氟会使化合物的性质带来意想不到的变化。近年来,发展向分子中高效、绿色引入氟的方法得到化学家的广泛关注,并取得了重要的进展。向芳香烃中引入氟是主要的研究方向之一,如何直接不对称地构筑碳-氟烷基键(C-RF)高对映选择性地形成手性中心的研究十分少见,存在很大的挑战。
三氟甲基作为重要的官能团,广泛存在于医药、农药和材料分子中,许多药物分子中包含三氟甲基手性中心。该手性中心是通过含有三氟甲基的潜手性化合物转化得到。到目前为止,直接不对称催化三氟甲基化的报道较少,主要集中在有机分子催化醛、酮、亚胺和Morita–Baylis–Hillman类型的不对称亲核三氟甲基化以及羰基α位的不对称亲电或自由基三氟甲基化。然而,这些方法都局限于羰基化合物的不对称三氟甲基化,从化合物结构多样性角度来看,过渡金属催化的不对称三氟甲基化是一种高效、简洁直接构筑C-CF3键产生手性中心的策略。但是这一策略至今没有实现,存在很大挑战,主要是由于缺乏合适的催化体系。

中国科学院上海有机化学研究所的张新刚(点击查看介绍)课题组长期致力于过渡金属催化氟烷基化反应的研究(Org. Lett., 2012, 14, 1938; Angew. Chem. Int. Ed., 2014, 53, 1669; Angew. Chem. Int. Ed., 2014, 53, 10457; Nat. Chem., 2017, 9, 918)。近期,该课题组以光学活性的炔丙基磺酸酯为底物,在铜的催化下首次实现了TMSCF3对炔丙基位立体专一性的三氟甲基化反应。该反应底物适用性广、效率高、官能团兼容性好,而且具有优秀的立体专一性(93-99% ee, 0.93->0.99 es)和区域选择性(联烯副产物得到抑制)。其中,底物磺酸酯的选用对反应效率以及底物的稳定性十分重要,对甲氧基苯磺酸酯的效率最高,尽管甲磺酸酯作为底物也可以得到高反应效率,但由于稳定性不好,容易分解,没有得到进一步的利用。值得注意的是,该策略还可以拓展到立体专一性的二氟烷基化,从而体现出其适用性和广谱的底物兼容性。
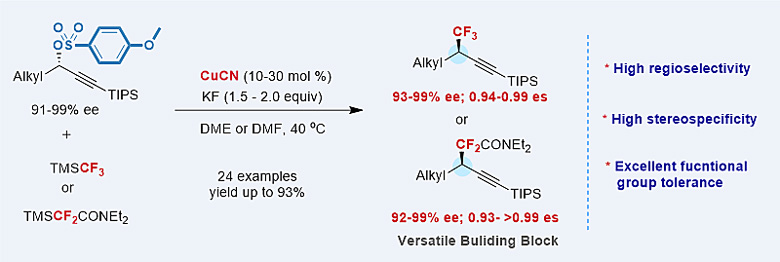
该反应的实用性还体现在得到的含氟化合物的后续转化上。例如以硅消除后的端炔产物8和9为模板底物,反应可以进行一系列的转化,合成各种具有高对映选择性的三氟甲基和二氟烷基化产物,这些化合物通常较难通过其他方法合成。

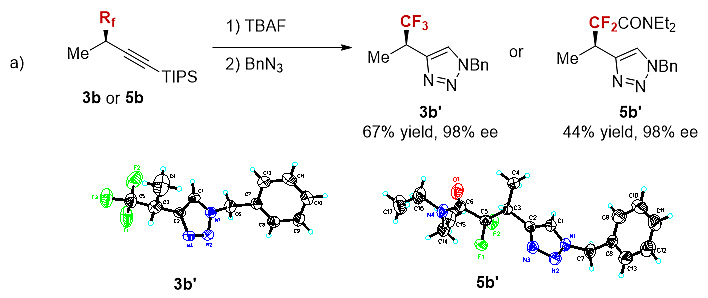
作者也对该反应机理进行了初步探讨。首先作者对产物的绝对构型进行了测定,将化合物3b、3e和5b消除硅保护基,直接与苄基叠氮进行[3+2]反应,得到固体化合物3b'、3e'和5b'。其X射线单晶结构表明,炔丙基手性中心的构型发生了翻转。根据以上实验结果和相关文献,作者提出了以下可能的机理:TMSCF3在KF的引发下与铜结合,产生CF3-Cu物种A。A与炔丙基磺酸酯发生SN2类型的氧化加成,产生构型翻转的铜物种Cu(III) B。最后,B经构型保持的还原消除得到与炔丙基磺酸酯构型相反的三氟甲基化产物。该研究在国家自然科学基金委的资助下,由中国科学院上海有机化学研究所的张新刚课题组高兴博士完成的,相关工作发表在Angew. Chem. Int. Ed. 上。

该论文作者为:Xing Gao, Yu‐Lan Xiao, Xiaolong Wan, Prof. Dr. Xingang Zhang
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Copper‐Catalyzed Highly Stereoselective Trifluoromethylation and Difluoroalkylation of Secondary Propargyl Sulfonates
Angew. Chem. Int. Ed., 2018, 57, 3187, DOI: 10.1002/anie.201711463
导师介绍
张新刚
http://www.x-mol.com/university/faculty/15617
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
上海有机所张新刚组Nature Chem.:从制冷剂到二氟甲基化试剂,挑战与突破 2017-03-20
-
钯催化下的氟烷基化插羰偶联反应 2017-01-06
-
铑催化下含氟芳烃选择性邻位C-F键活化硼化反应 2015-10-10
-
芳烃的直接一氟甲基化:镍催化下芳基硼酸与氟溴甲烷的偶联反应 2015-09-28
-
Copper-Catalyzed Enantioselective Trifluoromethylthiolation of Secondary Propargyl SulfonatesXing Gao, Yu-Lan Xiao, Shu Zhang, Jian Wu & Xingang Zhang1Key Laboratory of Organofluorine Chemistry, Center for Excellence in Molecular Synthesis, Shanghai Institute of Organic Chemistry, University of Chinese Academy of Sciences, Chinese Academy of Sciences, Shanghai 2000322School of Materials and Energy, University of Electronic Science and Technology of China, Sichuan 6117313College of Chemistry, Henan Institute of Advanced Technology, Zhengzhou University, Zhengzhou 450001


































 京公网安备 11010802027423号
京公网安备 11010802027423号