江苏师范大学石枫教授课题组Acc. Chem. Res.:有机小分子催化不对称合成吲哚类手性杂环化合物的策略、反应及展望
吲哚类手性杂环骨架是一类重要的杂环骨架,存在于许多具有重要生物活性的天然产物、药物分子、功能材料和手性催化剂或配体中,所以该类骨架的高效、高立体选择性构建已成为有机合成与药物研发领域的化学工作者们孜孜以求的目标之一。催化不对称合成,作为2001年诺贝尔化学奖的颁奖领域,已经成为合成手性化合物最高效的一种方法。因此,催化不对称合成吲哚类手性杂环骨架引起了化学工作者的强烈关注。但是,为了实现这一目标所发展的策略非常有限,在该领域仍然存在一些挑战性问题,例如:具有多种反应活性的平台分子的种类非常有限、具有原子和步骤经济性的催化不对称反应的类型非常有限、反应的立体选择性难以控制等。因此,非常迫切需要发展催化不对称合成吲哚类手性杂环骨架的新策略。
为了实现这一目标,江苏师范大学石枫教授(点击查看介绍)课题组近年来发展了一系列独特的策略,例如设计和开发具有多种反应活性的新型平台分子、以及它们参与的有机小分子催化的不对称反应,高效、高立体选择性地构建了多种吲哚类手性杂环骨架,工作总结最近发表在Acc. Chem. Res.。这篇综述系统地总结了该课题组为解决该领域存在的挑战性问题而采取的研究策略,主要包括:设计和开发了吲哚烯、吲哚醇、芳基吲哚和吲哚衍生物作为具有多反应活性的平台分子,用于构建具有结构多样性和复杂性的吲哚类手性杂环骨架;基于这些平台分子的性质,设计并实现了一系列有机小分子催化的不对称环加成反应、环化反应、加成反应和去芳构化反应,获得了高的原子经济性、步骤经济性和优秀的对映选择性。
通过这些策略,该课题组高效、高对映选择性地构建了结构复杂多样的吲哚类手性杂环骨架,包括五元至七元手性杂环骨架、轴手性杂环骨架和四取代手性杂环骨架。此外,该课题组还研究了一些吲哚类手性杂环化合物的性质,包括生物活性和催化活性,发现它们对多种肿瘤细胞具有显著的细胞毒活性、以及在不对称催化中具有一定的催化活性。这些结果为吲哚类手性杂环骨架的潜在应用提供了研究基础。
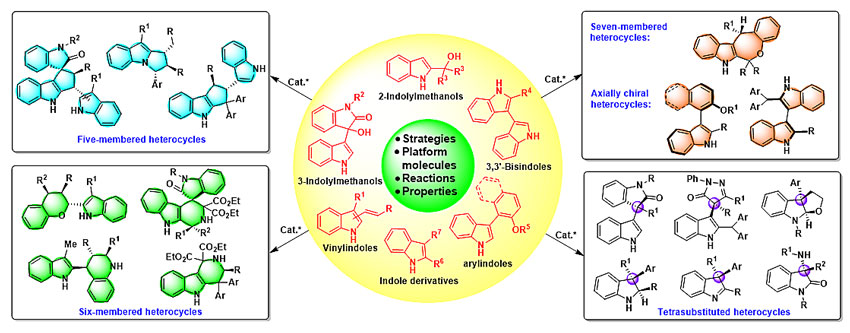
该综述的内容主要概括如下:
一、有机小分子催化不对称合成吲哚类手性杂环化合物的策略
1. 吲哚烯作为平台分子参与有机小分子催化的不对称反应
吲哚烯是催化不对称构建吲哚类手性杂环骨架的一类重要合成砌块,但是目前这一领域的研究工作仅限于2-吲哚烯以及3-吲哚烯作为4C合成砌块参与的催化不对称[4+2]环加成反应。石枫课题组设计并开发了两类新型的吲哚烯(3-烷基-2-吲哚烯和3-烷基-7-吲哚烯)作为平台分子,采用手性布朗斯特酸(B*-H)作为有机小分子催化剂,实现了新型吲哚烯作为2C合成砌块以及CCN合成砌块参与的不对称[3+2]、[4+2]环加成反应和[3+2]环二聚反应,高效、高对映选择性地构建了多种吲哚类手性杂环骨架(图1)。例如,通过3-烷基-2-吲哚烯参与的催化不对称氧杂Diels−Alder反应,实现了含有吲哚母核的手性六元杂环骨架的催化不对称构建 (Angew. Chem. Int. Ed., 2015, 54, 546)。
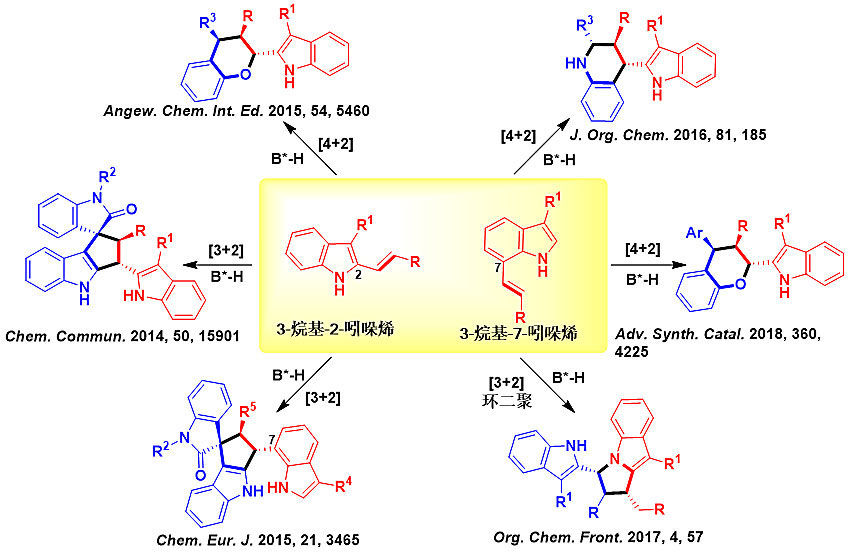
图1. 基于新型吲哚烯参与的催化不对称反应构建吲哚类手性杂环骨架
2. 吲哚醇作为平台分子参与有机小分子催化的不对称反应
吲哚醇作为一类重要的合成砌块被广泛应用于吲哚类手性杂环骨架的催化不对称构建,在近十年中,3-吲哚醇参与的催化不对称反应得到迅速发展。石枫课题组开发了3-吲哚醇作为平台分子,实现了手性布朗斯特酸催化下该类平台分子参与的多种不对称加成反应和[3+2]、[3+3]环加成反应,构建了结构多样的吲哚类手性杂环骨架(图2)。
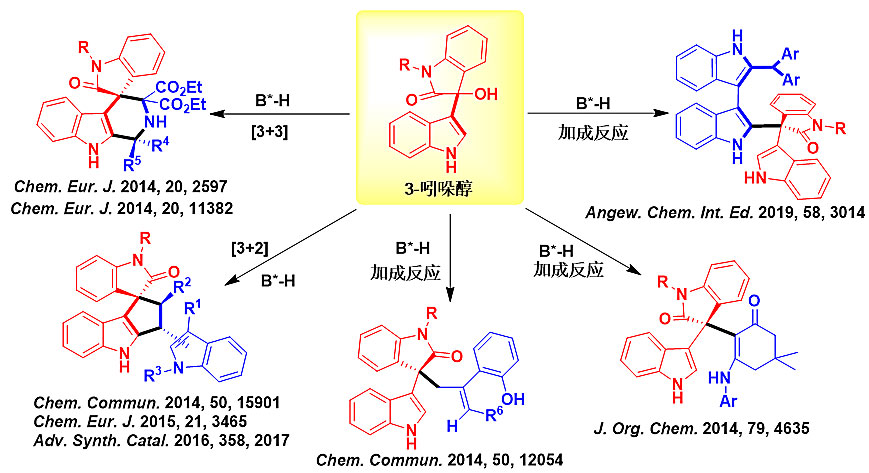
图2. 基于3-吲哚醇参与的催化不对称反应构建吲哚类手性杂环骨架
与3-吲哚醇参与的催化不对称反应相比,2-吲哚醇参与的催化不对称反应发展非常缓慢。石枫课题组开发了2-吲哚醇作为平台分子,发现了2-吲哚醇C3-位的极性反转现象,实现了一系列手性布朗斯特酸催化下2-吲哚醇参与的不对称[3+2]、[3+3]、[4+3]环加成反应和加成反应,构建了多种吲哚类手性杂环骨架(图3)。例如,通过2-吲哚醇参与的催化不对称加成反应,实现了新型芳基吲哚轴手性骨架的催化不对称构建 (Angew. Chem. Int. Ed., 2017, 56, 116),通过2-吲哚醇参与的催化不对称[4+3]环加成反应,实现了吲哚并手性七元杂环骨架的催化不对称构建 (Angew. Chem. Int. Ed., 2019, 58, 8703)。

图3. 基于2-吲哚醇参与的催化不对称反应构建吲哚类手性杂环骨架
3. 芳基吲哚作为平台分子参与有机小分子催化的不对称反应
催化不对称构建轴手性骨架近年来受到化学工作者的强烈关注,但是构建的大部分骨架是轴手性二芳基骨架。而催化不对称构建轴手性杂芳环骨架,尤其是轴手性五元杂芳环骨架的例子,却非常有限,这是由于该类骨架的旋转能垒较低、构象的稳定性较差。因此,该类骨架的催化不对称构建具有很大的挑战性,非常迫切需要发展催化不对称构建轴手性五元杂芳环骨架的策略。
为了实现这样一个目标,石枫课题组开发了芳基吲哚作为一类新型的平台分子,用于催化不对称构建轴手性五元杂芳环骨架 (图4)。例如,采用3,3'-双吲哚作为平台分子在手性布朗斯特酸催化下,与多种大位阻的亲电试剂(如3-吲哚醇)发生不对称加成反应,构建了同时具有轴手性和中心手性的3,3'-双吲哚骨架(Angew. Chem. Int. Ed., 2019, 58, 3014);采用消旋的萘基吲哚或苯基吲哚在手性布朗斯特酸催化下,与多种大位阻的亲电试剂(如偶氮酯、邻羟基苄醇)发生加成反应,通过动态动力学转化过程得到轴手性的芳基吲哚骨架 (Angew. Chem. Int. Ed., 2019, 58, 15104)。
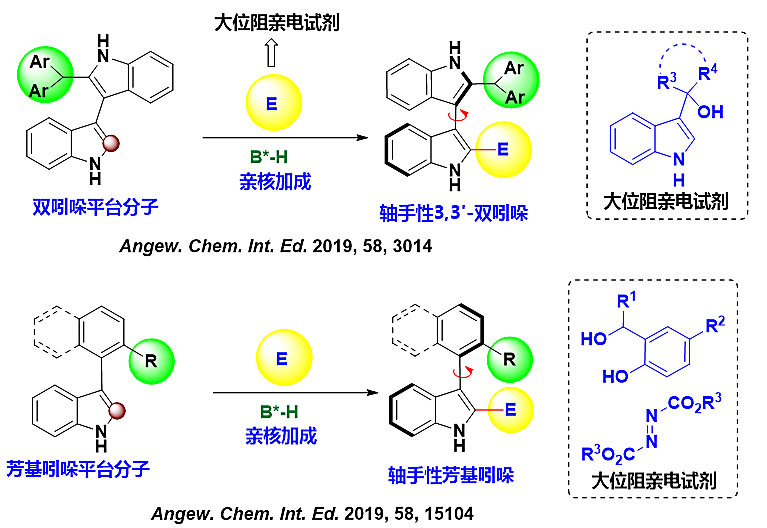
图4. 基于芳基吲哚参与的不对称反应构建轴手性吲哚骨架
4. 吲哚衍生物的催化不对称去芳构化反应
吲哚衍生物的催化不对称去芳构化反应是合成四取代手性吲哚衍生物的有效方法之一,但是吲哚衍生物的芳基化去芳构化反应却鲜有报道。石枫课题组发展了有机小分子催化下2,3-二取代吲哚、色醇等吲哚衍生物的不对称芳基化去芳构化反应,构建了多种手性四取代吲哚骨架(图5)。例如,利用2,3-二取代吲哚的催化不对称芳基化去芳构化反应,构建了两类手性四取代吲哚骨架 (Angew. Chem. Int. Ed., 2014, 53, 13912)。

图5. 基于吲哚衍生物参与的催化不对称去芳构化反应构建手性四取代吲哚骨架
二、吲哚类手性杂环化合物的性质
石枫课题组研究了部分吲哚类手性杂环化合物性质,主要包括生物活性和催化活性。通过研究,发现一些吲哚类手性杂环化合物对肿瘤细胞MCF-7、A549、788-0、BT474具有较好的抑制效果(图6a)。此外,轴手性吲哚骨架还可以转化成轴手性的三芳基膦衍生物,它们可以作为手性膦催化剂催化一些环加成反应(图6b)。

图6. 部分吲哚类手性杂环化合物的生物活性及催化活性
三、展望
有机小分子催化下吲哚类手性杂环化合物的合成无疑已成为和继续成为不对称催化与合成领域的一个热点问题,这是由于:(1)吲哚类手性杂环骨架广泛存在于生物活性分子中,需要进一步发展立体选择性构建该类骨架的方法;(2)基于这些新型的轴手性芳基吲哚骨架,可以设计和开发优势的手性催化剂和配体;(3)通过这些方法可以得到大量的手性吲哚衍生物的化合物库,用于生物活性筛选,以发现手性先导化合物。石枫课题组在此综述中的工作总结,不仅将为发展有机小分子催化不对称合成吲哚类手性杂环化合物的策略提供一个新的视野,而且将激励全世界的化学家为解决该领域中存在的挑战性问题而继续努力,促进该领域的繁荣和发展。
该工作总结发表在Acc. Chem. Res.,张宇辰副教授为第一作者,石枫教授为通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Organocatalytic Asymmetric Synthesis of Indole-Based Chiral Heterocycles: Strategies, Reactions, and Outreach
Yu-Chen Zhang, Fei Jiang, Feng Shi*
Acc. Chem. Res., DOI: 10.1021/acs.accounts.9b00549
导师介绍

石枫,江苏师范大学化学与材料科学学院副院长、教授,《有机化学》第一届青年编委、江苏省杰出青年基金获得者、江苏省“333高层次人才”中青年学术技术带头人、江苏省“六大人才高峰”高层次人才、江苏省高校“青蓝工程”中青年学术带头人。主要从事催化不对称合成手性杂环分子的研究,为构建结构复杂多样的手性生物活性杂环骨架提供了高效的方法。以通讯作者在Acc. Chem. Res.、Angew. Chem. Int. Ed. (7篇)、ACS Catal.(2篇)、Org. Lett.、Chem. Commun.、Org. Chem. Front.、Adv. Synth. Catal.、J. Org. Chem. 等刊物发表学术论文116篇。以第一发明人申请发明专利5项,授权发明专利1项。荣获江苏省科学技术二等奖、教育部自然科学二等奖、Thieme Chemistry Journal Award、Asian Core Program Lectureship Award等奖项。
课题组主页
https://www.x-mol.com/groups/Shi_Feng
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号