香港大学汪卫平团队JACS:长波长光分解前药的单光子光解策略
光控释药技术能够在光激发下控制药物的释放,从而实现定点定时给药,提高治疗效果。然而这一技术受限于常用激发光在生物组织中有限的穿透深度。近日,香港大学的汪卫平教授团队,通过构建光敏剂与光解分子之间的能量传递,研发了一种类似上转换发光光解的单光子光解策略,使前药的激发波长由绿光延长到了红光。由于长波长光具有更强的生物组织穿透力和更低的光毒性,因此这项研究在生物医学中具有广阔的应用前景。
光解反应可在光激发下释放功能性分子,实现在时间-空间上的控释,是一种在化学、生物和医学领域具有广泛应用前景的光学工具。在生物医学应用中,因为长波长光具有更强的组织穿透力和更低的光毒性,许多工作都致力于延长光解反应的激发光波长。到目前为止,能够被比吸收波长更长的光激发的光解反应都是通过多光子过程实现的,包括双光子吸收和上转换发光。然而,这类多光子过程需要用到高能量的激光激发或者需要用到多种成分作为能量传递的中间体,从而限制了这类技术的临床应用。
研究团队借助比光解分子具有更低单线态激发态(S1)和更高三线态激发态(T1)能级的光敏剂,通过构建光敏剂和光解分子之间的三线态-三线态能级传递(TTET),使光解分子达到T1态,进而使其发生分解并释放功能性分子(图1)。由于光敏剂具有更低的S1态能级,因此上述过程可以使用比光解分子吸收波长更长的光来激发。为了证明上述策略的可行性,该研究团队将四苯基苯并卟啉铂(PtTPBP)和一种基于二吡咯亚甲基二氟化硼(BODIPY)的前药分别选为光敏剂和光解分子。正常情况下,前药只能被绿光分解。但加入PtTPBP后,低功率的红光LED就能使前药分解并释放出抗癌药物苯丁酸氮芥。另外,通过利用这一策略还能在其他特定的前药上获得比直接使用绿光激发更高的光解量子效率。这一结果还从未在基于多光子策略的光解过程中实现过。
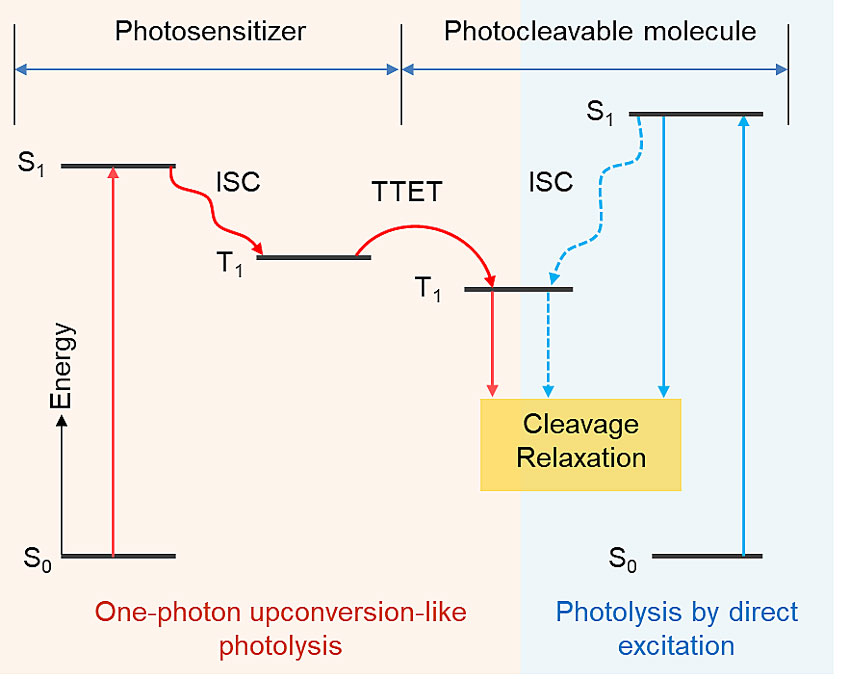
图1. 单光子光解新策略(红线)和直接使用吸收光激发的光解反应(蓝线)能级示意图。图中省略了其余的激发态弛豫过程。S0:单线态基态,S1:单线态激发态,T1:三线态激发态,ISC:系间窜越,TTET:三线态−三线态能量传递。
该项研究成果近期发表在Journal of the American Chemical Society 上,文章通讯作者为香港大学的助理教授汪卫平博士,第一作者是香港大学博士后吕雯博士,基于该成果的PCT申请已经提交。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Upconversion-like Photolysis of BODIPY-Based Prodrugs via a One-Photon Process
Wen Lv, Yafei Li, Feiyang Li, Xin Lan, Yaming Zhang, Lili Du, Qiang Zhao, David L. Phillips, Weiping Wang
J. Am. Chem. Soc., 2019, 141, 17482-17486, DOI: 10.1021/jacs.9b09034
汪卫平博士简介

汪卫平博士,香港大学李达三博士研究中心和李嘉诚医学院药理及药剂学系助理教授。2011年于香港科技大学获得博士学位后,在麻省理工学院和哈佛医学院从事博士后工作,2016年任香港大学助理教授、博士生导师。
汪卫平博士在香港大学所主持的分子工程与纳米医学实验室,主要基于分子设计与组装、光化学及纳米技术,组建刺激响应型分子/纳米系统、药物输送载体及功能生物材料等,致力于癌症治疗、眼睛疾病治疗及再生医学等应用上的研究。已在JACS,Nano Lett,Nano Today,Nature Commun 等国际期刊发表论文28篇,其中五篇被遴选为封面文章;获授权国际专利2项,申请PCT专利1项。获得的重要奖项包括国际知名期刊Nano Research 2018年度纳米研究青年创新奖、国际先进材料学会2018年科学家奖章以及世界华人生物医学工程协会2011年青年研究者奖等。
实验室网址
香港大学官网报道
https://www.hku.hk/press/press-releases/detail/c_20113.html
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!































 京公网安备 11010802027423号
京公网安备 11010802027423号