有机电合成:烯烃双胺化
1,2-二胺结构广泛存在于天然产物、药物和不对称合成所使用的催化剂中。烯烃双胺化,即在烯烃两端同时引入两个氨基,是合成1,2-二胺最为简便和高效的方法之一。但该方法面临着诸多挑战,是有机合成中有待解决的难题。其难点主要源于二胺产物对过渡金属催化剂的抑制作用以及难以控制反应的非对映选择性和区域选择性。
厦门大学徐海超(点击查看介绍)课题长期致力于有机电合成研究,该课题组近期对电化学促进的烯烃双官能团化反应进行了深入研究,并且已经通过电合成方法实现了烯烃与二醇的脱氢环化反应(Nat. Commun., 2018, 9, 3551),为饱和氧杂环提供了高效的合成途径。在此基础上,该课题组实现了烯烃与磺酰胺的脱氢环化反应,通过进一步脱除磺酰基,成功实现了高非对映选择性和区域选择性的烯烃双胺化反应,为1,2-二胺类化合物提供高效、简便的合成方法。
该反应适用于一系列二取代以及三取代内烯烃,并且均能取得较高的dr值。对具有不同电性取代基的芳环均有较好的兼容度,并且底物中所含有的多种官能团均能不受影响,其中在电氧化条件下极易被过度氧化的烷基胺能在强酸保护下而完好兼容。与此同时,该反应还能用于部分天然产物的后期官能团修饰。
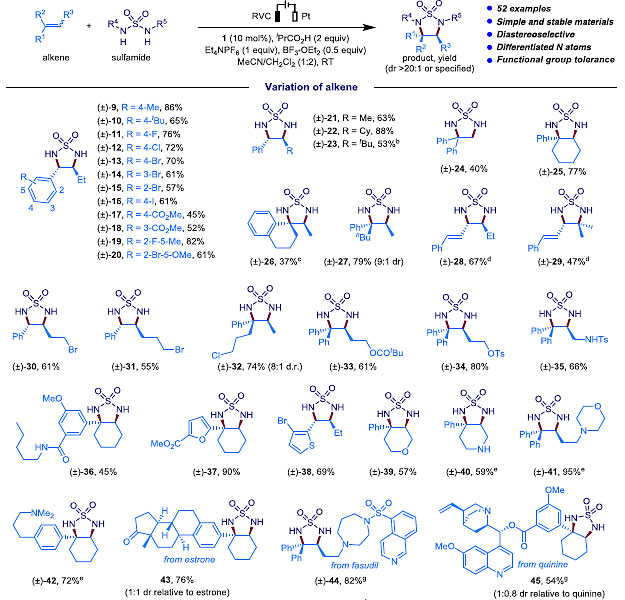
通过使用单取代的磺酰胺作为原料,可实现具有两个不同胺基的二胺化合物的合成。并且,使用环状磺酰胺可以制备桥环二胺结构底物。

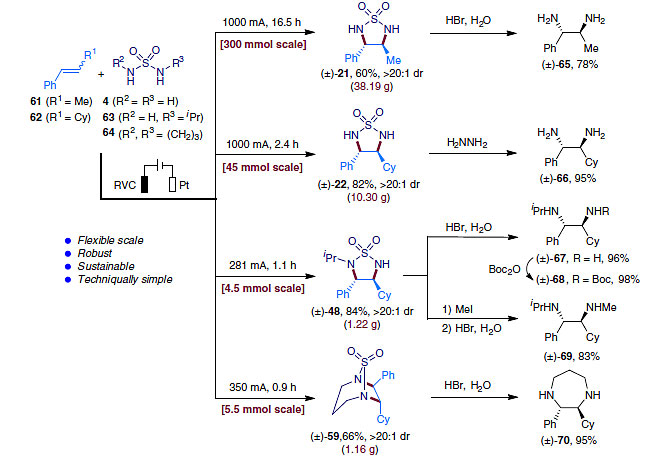
该反应可以轻易地实现0.3 mol规模的放大,并且产率与小量相差无几。通过对磺酰胺的脱除,能够以高产率得到二胺化合物。
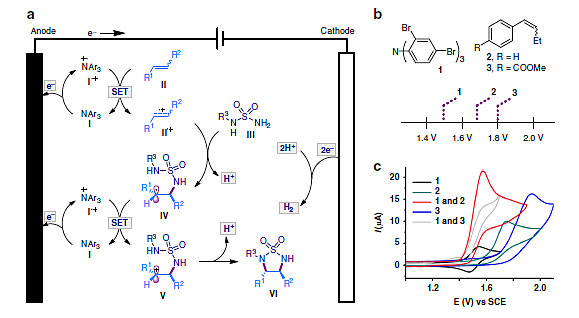
该工作通过有机电子转移催化剂与电的结合避免了过渡金属催化剂和氧化剂的使用,且增强了底物和官能团的兼容性。该催化剂参与的间接氧化使得基于电极表面电子传递产生高活性自由基正离子的方式转变为于溶液本体的氧化过程,从而避免了由于自由基正离子局部浓度过高而产生的一系列副反应,也进一步缓和了电极钝化的问题。
综上所述,本文在电化学条件下,通过对烯烃的氧化产生自由基正离子这一活性中间体,实现了烯烃与磺酰胺的脱氢环化反应,具有较高的区域选择性和非对映选择性,无需当量氧化剂和过渡金属催化剂。相关成果在线发表于Nature Communications,并被选为Editors'Highlights论文。文章的第一作者为厦门大学博士研究生蔡晨燕。该研究工作得到国家重点研发计划纳米科技重点专项(项目批准号:2016YFA0204100)、国家自然科学基金(项目批准号:21672178)、长江学者和创新团队发展计划、中央高校基本科研业务费专项资金的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Practical and stereoselective electrocatalytic 1,2-diamination of alkenes
Chen-Yan Cai, Xiao-Min Shu, Hai-Chao Xu
Nat. Commun., 2019, 10, 4953, DOI: 10.1038/s41467-019-13024-5
导师介绍
徐海超
https://www.x-mol.com/university/faculty/14206
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号