唐本忠院士团队深圳大学AIE研究中心JACS:近红外聚集诱导发光材料让革兰氏阳性菌无所遁形
近日,唐本忠院士(点击查看介绍)团队深圳大学AIE研究中心在Journal of the American Chemical Society 上发表论文,报道了一系列能够同时用于革兰氏阳性菌检测与高效光动力杀伤的双功能聚集诱导发光(AIE)材料,系统考察了分子结构与细菌成像和光动力抗菌效果之间的构效关系,并将综合性能优异的近红外聚集诱导发光探针用于大鼠皮肤伤口金黄色葡萄球菌感染的控制。
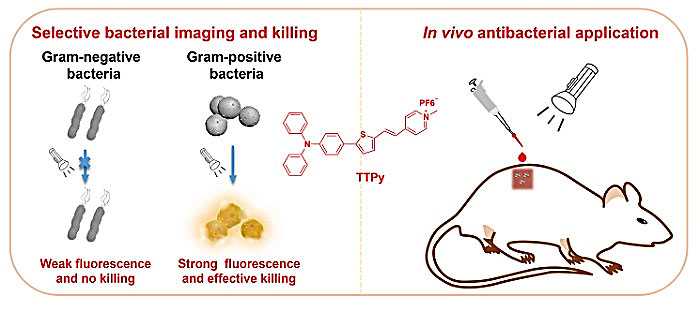
感染性疾病是全球范围内重要的公共卫生问题。细菌感染,尤其是革兰氏阳性菌感染严重威胁人类健康。细菌的快速检测和准确鉴别对于病原菌的检出和临床诊断具有重要作用。荧光成像技术具有灵敏度高、响应快速、背景噪音低、时空分辨率高、操作简单以及非侵入性等诸多优势,已成为当今生命科学领域最重要的技术手段之一。2001年,唐本忠院士首次提出“聚集诱导发光(AIE)”的新概念,引发了发光材料的革命,开启了一个由中国科学家提出并引领的研究新领域。不同于传统的有机荧光染料,AIE材料生物兼容性好、发光效率高、光稳定性好、斯托克斯位移大,可提供荧光“点亮型”检测。AIE材料在生物成像和治疗领域有显著优势,但兼具细菌区分与抗菌作用的长波长AIE材料的开发依然是一个挑战,分子结构与革兰氏阳性菌选择性成像和光动力杀伤效果之间的内在关系并不明朗。

图1. 分子结构及其细菌成像和在体抗菌应用示意图
近红外发光的荧光分子在生物应用中具有诸多优势,如穿透力强、对生物体的光损伤小,可避免生物体自发荧光的干扰,且能够大大减小光散射。在目前已有的报道中,近红外AIE分子的合成路径十分复杂,通常需要数步反应和繁琐的分离纯化步骤,这极大限制了AIE分子在生物医学领域的应用。在该工作中,王东副教授团队基于AIE这一创新性概念,通过强供电子基(D)和强吸电子基(A)的有效组合,发展了一系列合成简单、吸收和发射波长逐渐红移的AIE分子,其中TPy、MeOTTPy、TPE-TTPy均具有近红外荧光发射(图1,图2)。

图2. AIE分子的光物理学性质
为研究此类分子的细菌成像效果,作者分别选用金黄色葡萄球菌(革兰氏阳性菌)和大肠杆菌(革兰氏阴性菌)为代表。实验结果表明,正电性的AIE分子(TPy、TPPy、TTPy、MeOTTPy)能够选择性地对革兰氏阳性菌染色,对革兰氏阴性菌不染色,这是由于细菌表面负电性及革兰氏阳性菌和阴性菌被膜结构差异导致的(图 3a)。与商用的革兰氏阳性菌特异性荧光探针碘化乙啶HI相比,TTPy具有更优越的光稳定性。值得注意的是,TPE-TTPy对革兰氏阳性菌和阴性菌均不染色。作者对此进行了一系列研究,TPE-TTPy具有较大的空间位阻、较高的脂水分配系数(Clogp,9.02)和较小的临界聚集浓度(CAC,1.8304 μM)(图3c),使得TPE-TTPy不易插入革兰氏阳性菌相对疏松的细胞被膜进行染色,Zeta电势结果进一步证实了以上结论(图3b)。

图3. AIE分子的革兰氏阳性菌选择性成像及机理解释
除此之外,此类分子还具有较高的活性氧(ROS)产生效率(图4a)。以TTPy为例,浓度低至1 μM,白光照射30 s后,ROS指示剂DCFH的荧光强度即增强至初始值的1000倍左右,表现出超高的ROS产生效率,远优于现有的商用光敏剂(图 4b)。得益于其超高的ROS产生效率,TTPy能够高效光动力杀伤金黄色葡萄球菌,对大肠杆菌几乎无影响(图4c-e)。

图4. ROS的产生及TTPy对革兰氏阳性菌的高效光动力杀伤作用
进一步地,作者建立了大鼠背部皮肤金黄色葡萄球菌感染的伤口模型(图5)。各组给予不同处理后,取对应伤口处组织、匀浆、进行细菌培养和菌落计数,结果表明,光动力治疗实验组的细菌菌落数量几乎为零,明显少于对照组。H&E染色结果显示,光动力治疗实验组的中性粒细胞数量明显少于对照组。充分表明了TTPy对于革兰氏阳性菌具有优异的光动力抗菌疗效,能够在体控制金黄色葡萄球菌引起的感染。

图5. 大鼠皮肤伤口感染模型及TTPy的在体抗菌效果
综上所述,此研究发展了一系列简易合成的多功能深红/近红外AIE分子,具有光稳定性强、革兰氏阳性菌靶向性好、ROS产生效率高、光动力抗菌效果好等优势;深入探究了AIE分子的结构与细菌成像和光动力抗菌效果之间的构效关系,并将优化的聚集诱导发光分子,用于金黄色葡萄球菌的光动力杀伤、以及大鼠皮肤伤口金黄色葡萄球菌感染的控制,收到良好的效果。此工作报道了第一例用于在体实验的具有革兰氏阳性菌靶向成像和高效光动力抗菌作用的双功能近红外AIE分子,将为更多用于临床研究和应用的新型长波长细菌感染性疾病诊疗一体化材料的开发提供理论指导。
该论文的第一作者是深圳大学AIE研究中心康苗苗博士,共同第一作者为香港科技大学周成成博士。深圳大学AIE研究中心执行主任王东副教授为论文第一通讯作者,深圳大学材料学院王雷教授及AIE研究中心荣誉主任唐本忠院士为共同通讯作者。该论文得到了北京化工大学徐福建教授、俞丙然副教授、吴双梅同学,深圳大学张志军博士、宋楠博士,香港科技大学李美雪同学、许文涵同学的支持和帮助。该研究得到国家自然科学基金委及深圳大学自然科学基金等经费支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Evaluation of Structure-Function Relationships of Aggregation-Induced Emission Luminogens for Simultaneous Dual Applications of Specific Discrimination and Efficient Photodynamic Killing of Gram-Positive Bacteria
Miaomiao Kang, Chengcheng Zhou, Shuangmei Wu, Bingran Yu, Zhijun Zhang, Nan Song, Michelle Mei Suet Lee, Wenhan Xu, Fu-Jian Xu, Dong Wang, Lei Wang, Ben Zhong Tang
J. Am. Chem. Soc., 2019, 141, 16781-16789, DOI: 10.1021/jacs.9b07162
导师介绍
唐本忠
https://www.x-mol.com/groups/tang_benzhong
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号