分子识别构筑多功能纳米药物
多功能纳米药物集靶向、治疗、成像于一体,近年来在癌症的诊断治疗中表现出巨大的潜力和广阔的临床应用前景。近日,上海交通大学的张川研究员(点击查看介绍)和朱新远教授(点击查看介绍)研究团队通过核酸碱基分子识别构建了一种新型的多功能纳米药物,可用于癌症的靶向治疗。
与传统的纳米药物相比,多功能纳米药物输送体系在肿瘤治疗中具有更大的优势。例如,多功能纳米药物中的主动靶向组分可以提高纳米药物的特异性以及在肿瘤部位的积累,穿膜组分能够增强纳米药物进入细胞的能力,造影剂能定位纳米药物的输送过程及药物剂量。这些组分的引入增强了药物的输送效率,有效提高了药物的生物利用率。尽管目前已报道的多功能纳米粒子能有效提高纳米药物的治疗效果,但是设计和制备能够满足临床需求的多功能纳米药物体系仍旧是一大难题。首先,多功能纳米体系的合成复杂繁琐,每一种功能性单元的引入大多都需要复杂的合成、分离纯化以及分析表征,产率低、成本较高;其次,多功能纳米药物的构建大多涉及到聚合物,而聚合物本身存在分子量分布,所以最终的多功能纳米药物体系存在批次差异的问题。
针对这些问题,上海交通大学的研究团队提出了利用自然界中最常见的分子识别来构建一类简单有效的多功能纳米药物体系,克服了传统多功能纳米药物制备复杂、成本高以及批次不稳定的难题。该研究利用低价高效的核苷类似物抗癌药物作为纳米药物的主体,通过碱基分子识别引入核酸适配体和DNA荧光探针分别作为靶向和成像组分,成功制备了具备靶向、成像和治疗功能的多功能纳米药物体系。
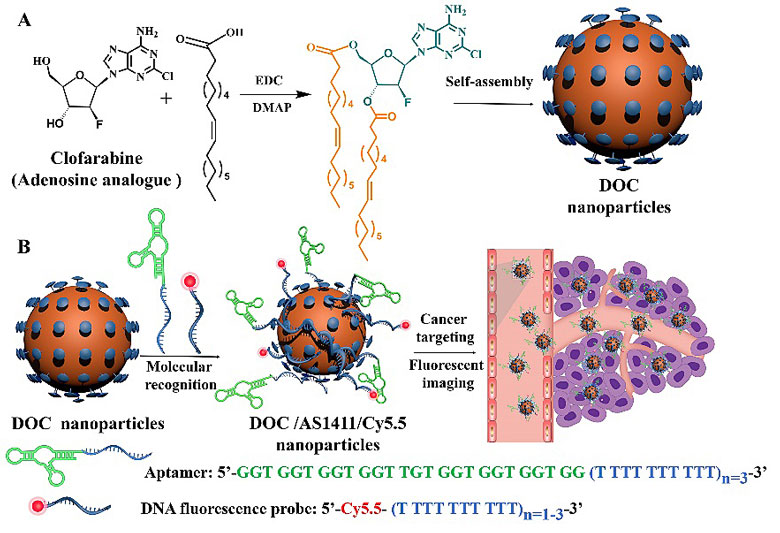
这种构建方法除了药物分子外仅需用到生物体大量存在的油酸和DNA分子,不仅有效避免了引入功能组分带来的复杂化学合成以及中间产物的纯化,而且产率较高,功能性组分可以根据需求进行自由调控,有利于实现其在临床医学上的个性化治疗。该方法具有普适性,可适用于几乎所有的核苷类似药物以及功能性核酸。此外,该研究的另一个创新点在于非常方便地实现了亲水性较强的核苷类似物抗癌药物纳米化制剂的制备。传统纳米药物输送体系大多以负载疏水性药物为主,进而实现药物的増溶、改善组织分布、降低毒性。而核苷类似物亲水性较强,生物体内扩散快,导致药物对正常细胞也具有很强的毒性,带来极大的副作用。将其通过自组装的方式制备成纳米化制剂能够充分利用纳米化效应、靶向效应,进而提高药效、降低毒性。因此,利用分子识别构建多功能的纳米药物为癌症的治疗提供了新的发展思路,在癌症的诊断和治疗上具有重大的意义。
相关研究成果已发表在Journal of the American Chemical Society 上,上海交通大学的王大力博士和哈尔滨医科大学的刘兵博士为并列第一作者。该工作受到国家自然科学基金、科技部国家重点基础研究发展计划的支持。
该论文作者为:Dali Wang, Bing Liu, Yuan Ma, Chenwei Wu, Quanbing Mou, Hongping Deng, Ruibin Wang, Deyue Yan, Chuan Zhang, Xinyuan Zhu
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Molecular Recognition Approach to Synthesize Nucleoside Analogue Based Multifunctional Nanoparticles for Targeted Cancer Therapy
J. Am. Chem. Soc., 2017, 139, 14021, DOI: 10.1021/jacs.7b08303
导师介绍
张川
http://www.x-mol.com/university/faculty/12622
朱新远
http://www.x-mol.com/university/faculty/12602
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!









































 京公网安备 11010802027423号
京公网安备 11010802027423号