余金权课题组Nature:无导向基团参与的芳基C-H键烯基化反应
C-H键官能化反应的研究最早可追溯至上世纪60年代,于90年代逐步得到有机化学领域研究者的密切关注。其中,有效克服C-H键的化学惰性并实现其区域选择性活化成为该类反应研究的难点。为此,人们发展了过渡金属参与的C-H键官能化反应,反应过程中形成C-M (M = 金属)键可以降低C-H键发生转化的活化能,从而提高其反应活性。而Naoto Chatani和Shinji Murai提出的导向基团策略则使该类反应的区域选择性得到很好的调控,他们通过在底物中修饰合适的配体基团,与过渡金属催化剂配位后,以特定的空间构型拉近过渡金属中心与底物中目标C-H键的距离并形成五元或六元环金属中间体,以此诱导C-H键选择性活化。随后人们在不同导向基团的研究与设计中做出了大量的工作,并寻找合适的配体对催化中心的空间及电子效应进行调控。尽管目前人们已通过导向基团策略实现底物分子中不同区域C-H键的选择性官能化,但反应前预修饰导向基团并后续消除会使反应过程大大繁琐,不仅在一定程度上限制了底物的适用范围,合成效率也因而受到影响。
近年来,发展无导向基团参与的C-H键官能化反应成为相关研究领域关注的焦点,该类反应不仅有望实现远程C-H键的活化,还可用于不适合修饰导向基团的底物。然而在底物中不存在导向基团时,C-H键活化过程中往往缺少底物与过渡金属中心的环金属化鳌合作用,其转化速率会大幅度降低,与此同时,由于缺少导向基团对过渡金属催化剂空间位置的控制,反应的选择性也会受到影响。例如,对于无导向基团参与的Pd催化芳基C-H键的官能化过程,人们需要大大提高底物的用量推动反应进行,C-H键官能化的区域选择性也仍需进一步改善,其中亲电钯化的芳香取代反应仅适用于富电子芳香烃底物。如何改变Pd催化剂的催化活性,提高反应的合成效率成为研究者需要思考的问题。
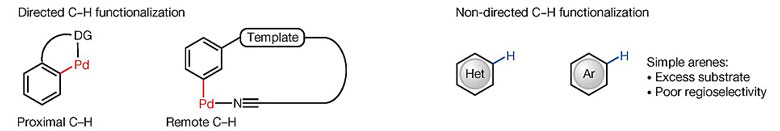
图1. 导向基团参与及无导向基团参与Pd催化的C-H键官能化反应。图片来源:Nature
最近,美国斯克里普斯研究所(The Scripps Research Institute, TSRI)的余金权(Jin-Quan Yu)教授(点击查看介绍)发展了一种配体促进的Pd催化芳基C-H键活化反应,他们设计了一种2-吡啶酮配体,与Pd催化剂结合后可以实现无导向基团参与的C-H键烯基化及羧化。反应对富电子及贫电子的芳香烃均具有较好的适用性,芳香烃可用作限制性试剂,合成效率与区域选择性得到极大地提升。除此之外,该反应还可用于杂芳香烃、氨基酸衍生物及其他复杂分子的C-H键官能化。相关研究成果发表在Nature 上,论文第一作者为王鹏(Peng Wang)博士。
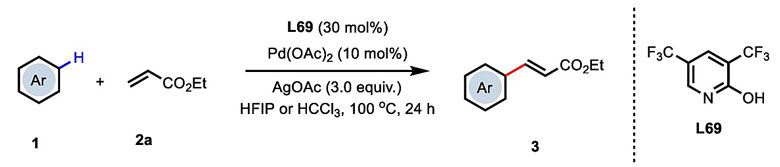
图2. 无导向基团参与Pd催化芳基C-H键的烯基化反应。图片来源:Nature
余金权教授在导向基团参与的C-H键官能化反应的研究中积累了大量的经验,发现调控配体的空间与电子特性可以改变催化剂的催化活性。他们首先以反应活性及选择性较差的1,2-二氯苯作为模板底物,丙烯酸乙酯作为烯基化试剂设计芳基C-H键烯基化反应,考察不同结构的配体对Pd(OAc)2配位后的催化活性。3-氨基-2-羟基吡啶L19参与配位后可以得到最佳的反应结果。随后作者对一系列羟基吡啶/吡啶酮结构进行筛选,3,5-二(三氟甲基)-2-羟基吡啶L69作为配体能以显著提高的收率得到目标产物,β/α选择性也得到明显的改善。他们进一步调整L19与烯基化试剂的用量,并结合不同Pd盐、氧化剂及溶剂对催化体系的影响,最终选择10 mol%的Pd(OAc)2作为Pd盐、30 mol%的L69作为配体、3.0当量的AgOAc作为氧化剂,使用2当量的丙烯酸乙酯参与烯基化过程,反应在HFIP溶剂中加热至100 ℃,以83%的分离收率得到1,2-二氯苯烯基化的产物,β/α选择性为3:1。
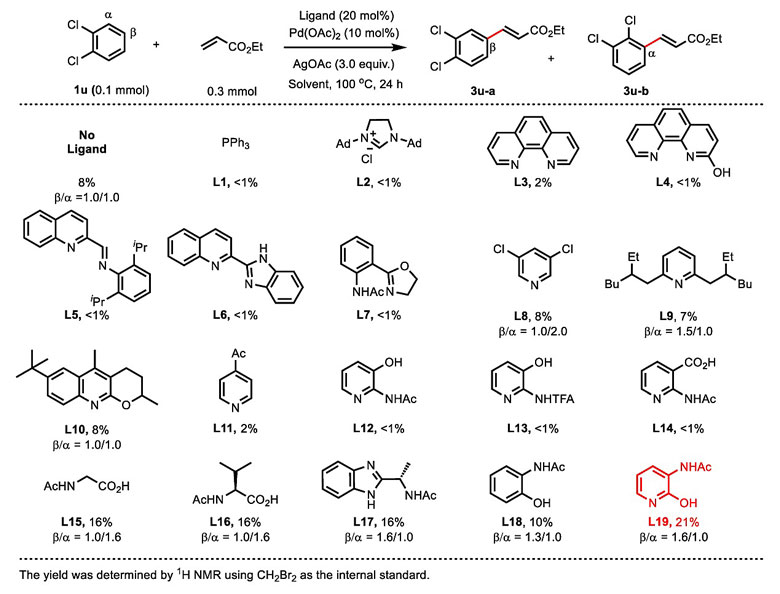
图3. 不同结构的配体对Pd(OAc)2配位后的催化活性。图片来源:Nature
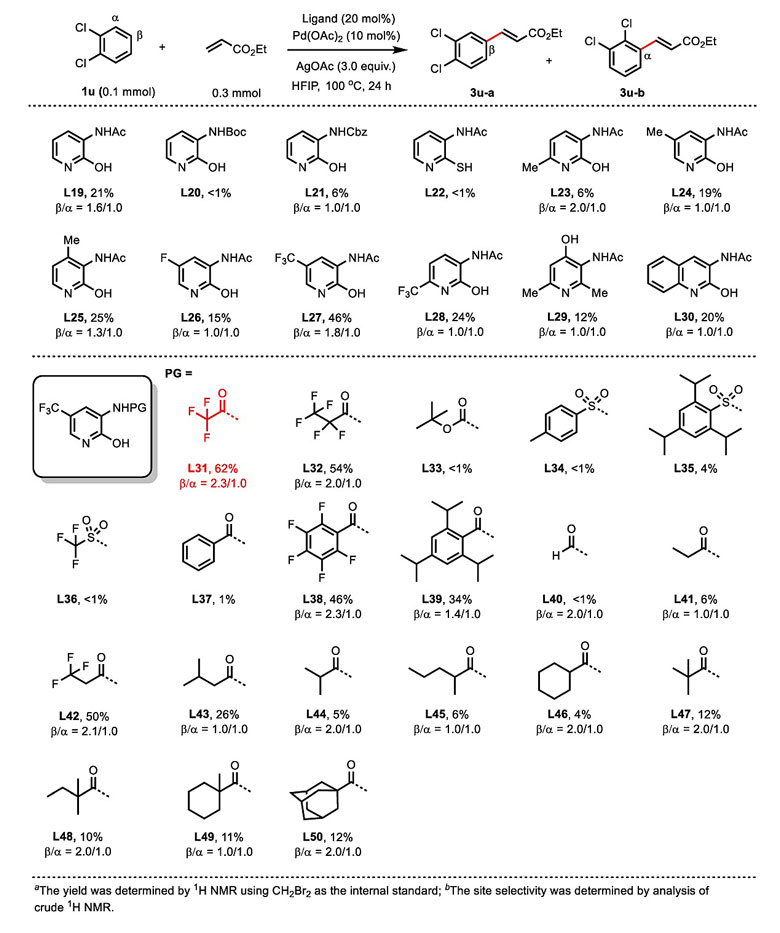
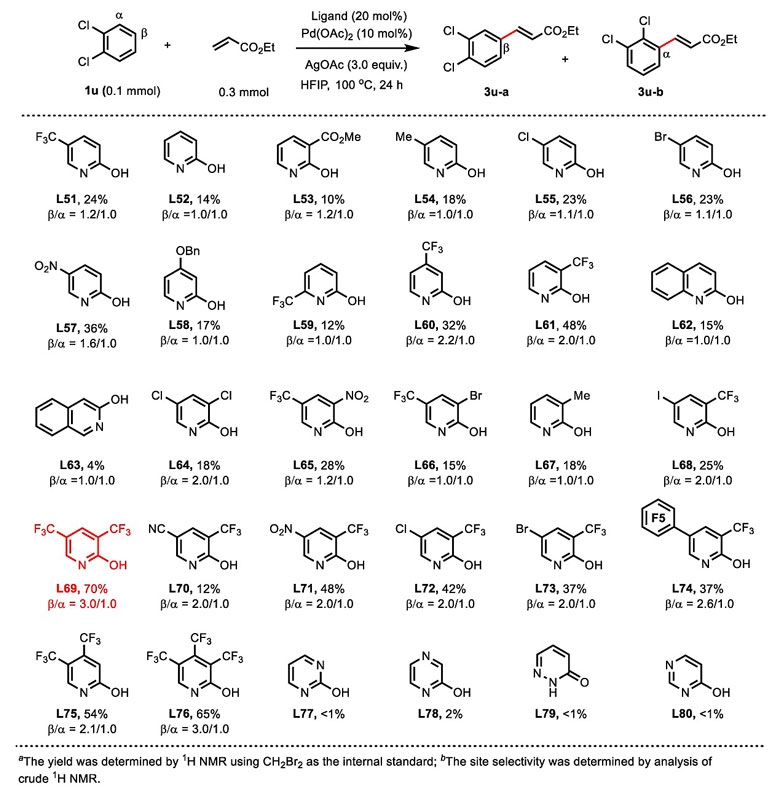
图4. 不同羟基吡啶/吡啶酮配体对Pd(OAc)2配位后的催化活性。图片来源:Nature
为了阐明L69对Pd催化剂活性产生影响的作用机制,作者首先通过X射线单晶衍射分析对Pd(Phen)(L69)2以及三聚体Pd3(μ2-OH)(L69)5配合物的结构进行表征,发现L69对Pd金属中心的配位方式与羧酸根类似。该结果与密度泛函理论(DFT)计算得出的反应过渡态优势构象中L69的配位方式一致。他们还选用苯作为模板底物,考察其与丙烯酸乙酯反应的动力学同位素效应(KIE, kH/kD = 2.9),说明C-H键断裂为决速步骤。动力学研究还表明,L69对Pd金属中心配位后,反应的初始速率得到显著的提高;与此同时,L69可有效抑制Pd活性物种聚合或分解,这种配体稳定作用对无导向基团参与芳香烃作为限制性试剂的C-H键活化反应的催化效率具有十分重要的影响。而体系中不加入配体L69时,贫电子的芳香烃不具有明显的反应活性,由此说明吡啶酮配体可能参与C-H键的断裂过程。这一假设同样得到DFT计算的支持,在最优过渡态中,两组吡啶酮配体同时与过渡金属中心配位,其中一组作为X型配体以к-2的方式与Pd结合,另一组则通过N原子与Pd作用,并进一步作为内源碱以协同的金属化-去质子化机理实现C-H键的断裂。
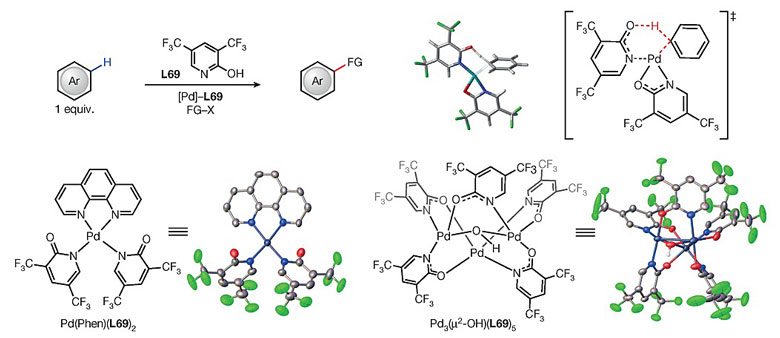
图5. 反应过渡态的DFT计算以及Pd(Phen)(L69)2、三聚体Pd3(μ2-OH)(L69)5配合物的X射线单晶衍射表征。图片来源:Nature
有了以上研究基础,作者以丙烯酸乙酯作为烯基化试剂考察不同芳香烃的底物适用范围,不同富电子及贫电子的芳香烃都能以中等至良好的收率得到单烯基化的产物,并具有良好的区域选择性。反应对多种官能团均具有良好的兼容性,部分高活性的底物参与反应时需以CHCl3作为溶剂减少二烯基化产物的生成。杂芳香烃、氨基酸衍生物以及其他复杂的生物活性分子也可以顺利地参与C-H键烯基化反应。随后他们又以邻二甲苯作为模板底物探究不同烯基化试剂的适用情况,α,β-不饱和烯烃可作为良好的烯基供体参与反应,修饰不同吸电子取代基的烯烃均能与反应体系很好地兼容。该反应同样可以实现克量级扩大规模的制备,配体L69可有效进行回收利用。作者还利用该催化体系初步建立了无导向基团参与的芳基C-H键羧化反应,但反应得到单羧化与二羧化的混合物,选择性仍需进一步改善。
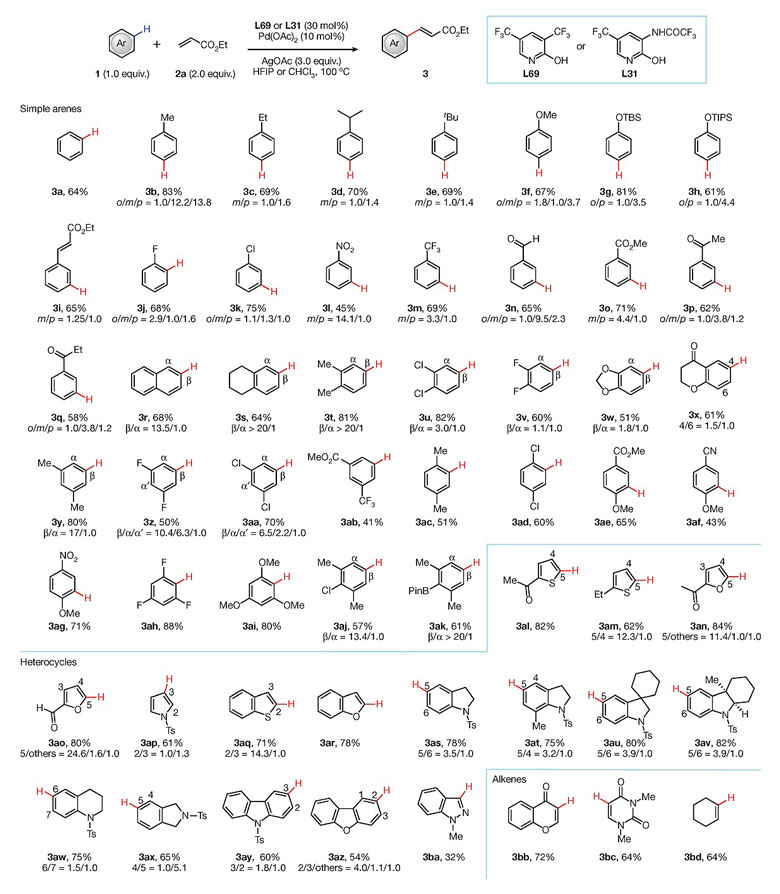
图6. 不同芳香烃底物适用范围的考察。图片来源:Nature
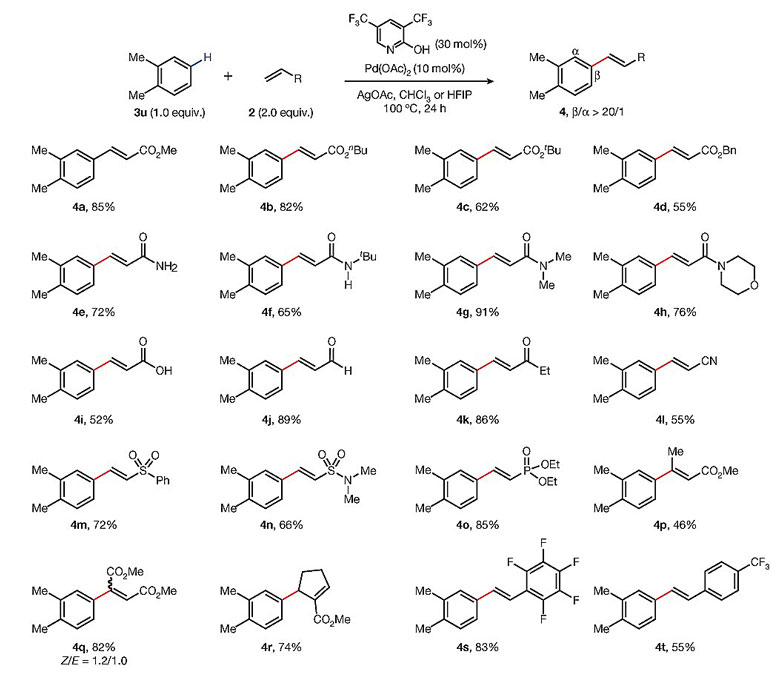
图7. 不同烯烃底物适用范围的考察。图片来源:Nature

图8. 氨基酸衍生物、天然产物及药物分子的C-H键烯基化反应。图片来源:Nature
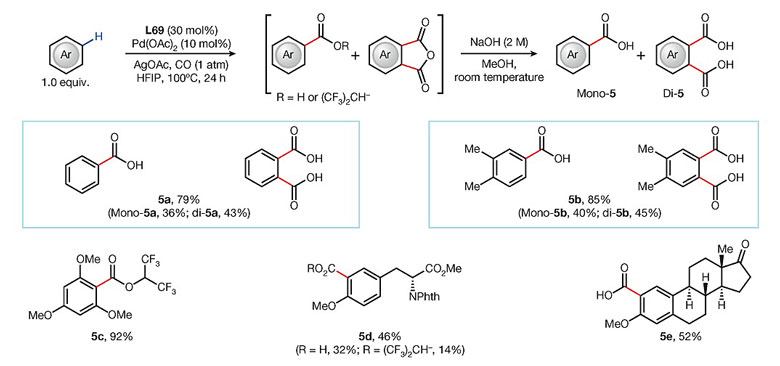
图9. 无导向基团参与Pd催化芳基C-H键的羧化反应。图片来源:Nature
——总结——
余金权教授发展了一种无导向基团参与的Pd催化芳基C-H键的烯基化反应。反应通过2-吡啶酮配体L69对过渡金属中心配位,并辅助参与C-H键断裂过程,实现了一系列富电子及贫电子芳香烃作为限制性试剂的C-H键高效官能化,并具有显著提高的区域选择性。该反应同样适用于其他杂芳香烃、天然产物及药物分子的后期修饰,有望在大规模的合成中得到广泛的应用。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Ligand-accelerated non-directed C–H functionalization of arenes
Nature, 2017, 551, 489, DOI: 10.1038/nature24632
导师介绍
余金权
http://www.x-mol.com/university/faculty/694
(本文由夜若岚尘供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!











































 京公网安备 11010802027423号
京公网安备 11010802027423号