止疼药变抗癌药——载酶MOF纳米反应器治疗癌症
化学疗法(chemotherapy)是目前治疗癌症的标准手段之一,通过化学药物抑制癌细胞的分裂和增殖等生理活动,直至最终癌细胞死亡。但是,化学药物会通过血液循环进入身体各处,在杀伤癌细胞的同时也会对正常细胞造成伤害,因此没有靶向作用的药物常常带来严重的副作用,像肾脏损伤、骨髓抑制、神经损伤、脱发、发烧、免疫力降低等等。另外,癌细胞常常会发展出抗药性,这也降低了化学疗法的抗癌效果。解决问题的一个策略是使用前体药物(prodrug,简称“前药”),前药无毒,但在肿瘤微环境中可被激活释放出具有细胞毒性的代谢物,从而选择性地杀伤肿瘤细胞。然而,这又会面临另一个挑战:确保前药的激活只针对癌细胞。目前,前药的活化一般依靠在癌细胞中过度表达的酶来实现。但是,这些用于活化前药的目标酶在正常细胞中也以低浓度存在,前药疗法往往很难成功。科研人员又想到在肿瘤中富集外源的激活酶,不过将它们选择性地富集在癌细胞同时还不被轻易降解,非常具有挑战性。
美国德克萨斯A&M大学的周宏才(Hong-Cai Zhou)教授课题组最近在Angew. Chem. Int. Ed.上报道了新突破,利用介孔金属有机框架(MOF)负载酪氨酸酶(tyrosinase,TYR)作为纳米反应器,活化了一种常见止疼药对乙酰氨基酚(paracetamol,APAP),使之变为具有细胞毒性的抗癌药,细胞实验以及小鼠实验均证明了这一策略良好的抗癌效果。
图1. 载酶MOF纳米反应器活化止疼药治疗癌症。
对乙酰氨基酚是一种非常常用的解热镇痛类非处方药物,用于缓解普通感冒或流行性感冒引起的发热,也用于缓解轻至中度疼痛如头痛、关节痛、牙痛等,是多种常见感冒药包括儿童用感冒药的主要活性成分。不过,这种药物经过酪氨酸酶的活化可以变成具有细胞毒性的苯醌类代谢物AOBQ。AOBQ可以使得细胞内活性氧族(ROS)水平升高,同时消耗谷胱甘肽(GSH),从而实现杀死癌细胞的效果(图2)。而选择仅在黑色素细胞和黑素瘤细胞中存在的酪氨酸酶作为活化酶,目的正是为了实现肿瘤特异性的前药活化。
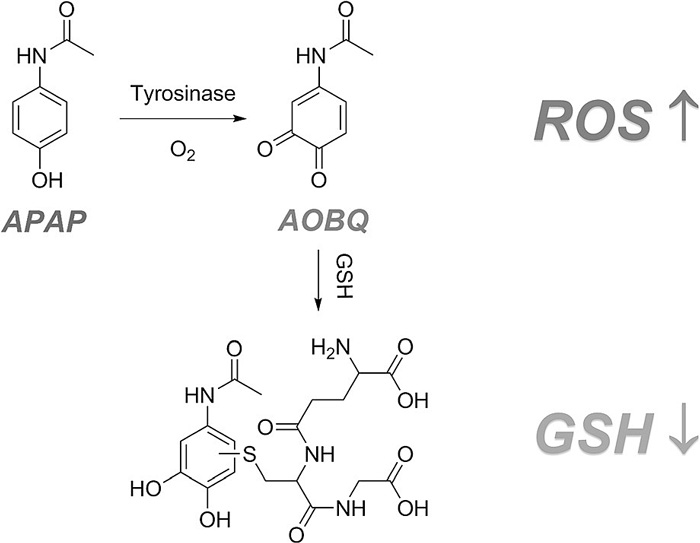
图2. 从APAP转化为具有细胞毒性的AOBQ机理图。图片来源:Angew. Chem. Int. Ed.
作者使用的MOF材料为PCN-333(Al),具有两类介孔,直径分别为4.2纳米和5.5纳米(图3a)。选中PCN-333的原因有三:酶负载能力高、易于用荧光团修饰(此后生物实验中便于追踪)、细胞环境中结构稳定。由于酪氨酸酶是一个比较大的酶,分子量43 kDa,尺寸约5.5 × 5.5 × 5.6 立方纳米,只有PCN-333直径5.5纳米的孔道能够容纳该酶(图3b)。将PCN-333的纳米颗粒(NPCN-333)与酪氨酸酶在溶液中混合20分钟后,酶的负载量达到了0.80 g/g,接近于理论负载量1.08 g/g。从孔径分布来看,负载酶的MOF——TYR@NPCN-333中的5.5纳米孔道被酶占据。
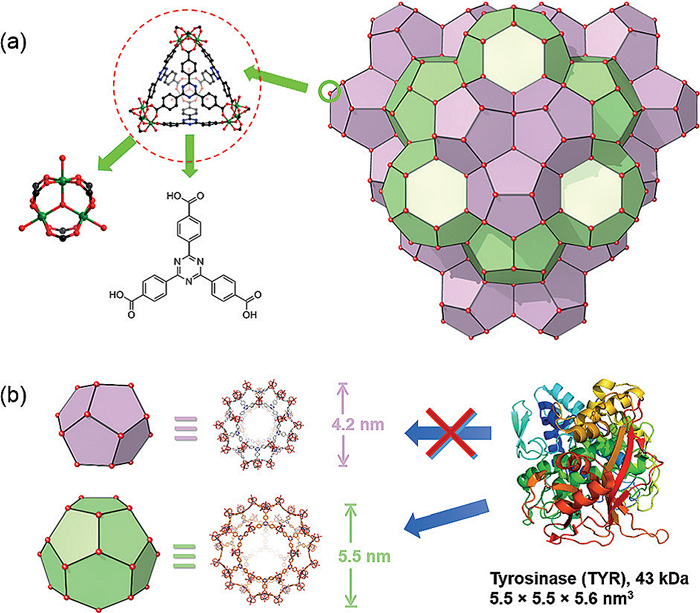
图3. PCN-333的结构和对TYR的负载。图片来源:Angew. Chem. Int. Ed.
作者使用紫外可见光谱表征了TYR@NPCN-333可以将APAP转化为AOBQ,证实这种载酶MOF纳米反应器保留了酶的活性。另外,他们也证实了MOF可以保护其中的酶不被胰蛋白酶降解,同时酸性环境(pH = 5)对酶活性也没有大影响,这些对于保持酶在细胞环境中的活性至关重要。接着,作者将TYR@NPCN-333引入对于顺铂以及其他常用抗癌药具有抗药性的卵巢腺癌细胞SKOV3-TR,以研究其抗癌活性。由于NPCN-333修饰上了荧光分子,这种载酶MOF纳米反应器进入细胞可以通过共聚焦显微镜追踪。作者发现,TYR@NPCN-333可通过细胞内吞进入癌细胞,随后聚集在内吞细胞器中。通过对比实验,仅有前药APAP或MOF纳米颗粒NPCN-333,都不会对癌细胞表现出杀伤力。然而,二者配合就表现出很强的细胞杀伤力(图4)。不仅对于卵巢腺癌细胞,这种载酶MOF纳米反应器可以在非小细胞肺癌H1299细胞和人宫颈癌HeLa细胞中同样活化前药APAP,起到良好的癌细胞杀伤效果。此外,TYR@NPCN-333预处理之后的SKOV3-TR细胞,在三天后加入前药APAP依然表现出很好的增殖抑制效果(50%)。而相比之下,游离的TYR预处理之后的SKOV3-TR细胞即刻加入前药APAP,癌细胞增殖抑制效果很一般,仅为20%;而且如果一天之后再加入前药APAP,则没有任何增殖抑制效果。这说明TYR@NPCN-333能在癌细胞中较长时间保持活性。
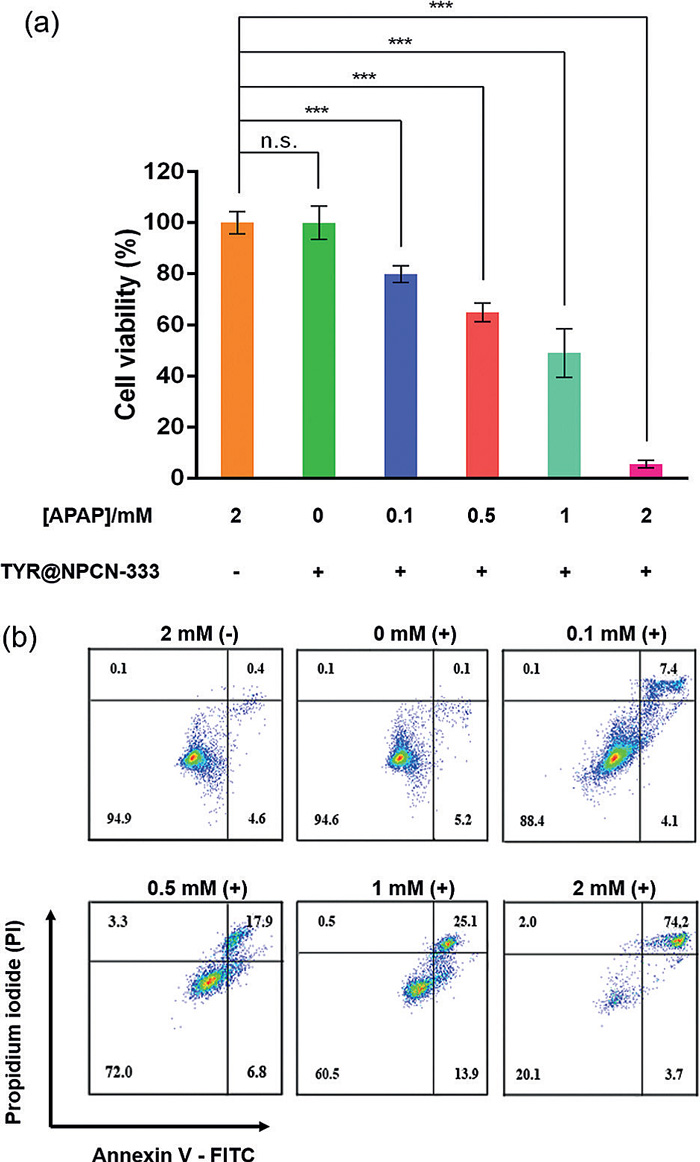
图4. 载酶MOF纳米反应器对癌细胞的活性。图片来源:Angew. Chem. Int. Ed.
然后,作者研究了TYR@NPCN-333在荷瘤小鼠模型中的抗癌效果。接受不同注射的小鼠肿瘤生长情况表明,相对于对照组,只有TYR@NPCN-333加APAP组呈现出良好的肿瘤抑制效果,小鼠体内肿瘤体积从约50立方毫米降到约20立方毫米(图5e),五只实验小鼠中有两只的体内肿瘤在实验结束时甚至完全消失了。仅有前药APAP或MOF纳米颗粒NPCN-333,或者在TYR@NPCN-333 + APAP组合中加入GSH,都没有类似效果。这说明,杀伤癌细胞的是载酶MOF纳米反应器对前药活化产生的可消耗GSH的代谢物,这与此前的机理预测相一致。
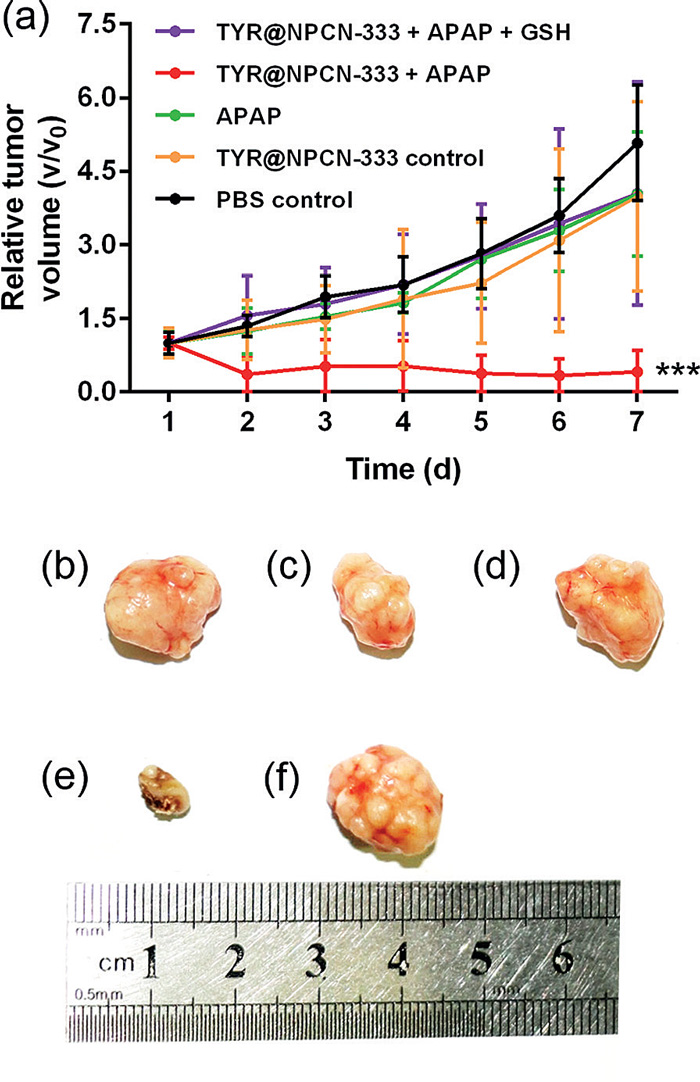
图5. 载酶MOF纳米反应器对在小鼠模型中的抗癌活性。图片来源:Angew. Chem. Int. Ed.
——总结——
周宏才教授课题组使用介孔MOF材料PCN-333纳米颗粒来负载酪氨酸酶得到TYR@NPCN-333纳米反应器,可在癌细胞内将无毒常用止痛药对乙酰氨基酚活化成具有细胞毒性的抗癌药,在细胞和动物实验中均展现出了良好的抗癌效果。通过MOF的稳定框架保护酶免于细胞环境内降解,保持酶的活性,把无毒的止疼药变为可治疗癌症的药物,这是一个很有希望的方法。近期使用MOF材料负载酶、DNA等生物活性物质的报道越来越多,希望研究者们开发出更多具有生物相容性的孔材料,用于生物医药方向的研究,造福人类社会。
相关工作近期发表在Angew. Chem. Int. Ed. 上,该工作的第一作者是刚刚毕业的廉玺祯(Xizhen Lian)博士,通讯作者是周宏才教授。该工作也得到同为德克萨斯A&M大学生物化学和生物物理学院的Jean-Philippe Pellois教授课题组的支持,动物活体实验部分得到了中科院北京化学研究所赵睿研究员课题组的帮助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Xizhen Lian, Yanyan Huang, Yuanyuan Zhu, Yu Fang, Rui Zhao, Elizabeth Joseph, Jialuo Li, Jean-Philippe Pellois, and Hong-Cai Zhou
Enzyme-MOF Nanoreactor Activates Nontoxic Paracetamol for Cancer Therapy
Angew. Chem. Int. Ed., 2018, 57, 5725-5730, DOI: 10.1002/anie.201801378
(本文由叶舞知秋供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号