结构生物学导向的非对称萘磺酰胺类Keap1-Nrf2抑制剂的设计
作者:X-MOL 2022-06-28
氧化应激(Oxidative stress)会导致慢性炎症,引起一系列的疾病如心血管疾病、败血症、肺炎、神经退行性疾病和癌症等等。Keap1−Nrf2系统是生物体抵御氧化应激的重要防御机制。作为重要的转录因子,Nrf2可以调节一系列氧化还原酶的转录,如血红素氧合酶1和NADPH: 醌氧化还原酶1等。泛素 E3 连接酶 Keap1 介导Nrf2的泛素化降解,在自由基等氧化压力存在时,Keap1介导的Nrf2的泛素化降解水平降低,导致Nrf2在细胞内的浓度升高,激活下游基因的表达,帮助细胞抵御氧化损伤。因此,一直以来,Keap1−Nrf2信号通路都是治疗氧化应激相关炎症和疾病的重要药物靶点。
近日,同济大学医学院附属第四人民医院许可教授团队与海军军医大学庄春林教授团队合作,以封面文章形式在Journal of Medicinal Chemistry上发表了研究论文,从抑制Keap1−Nrf2相互作用的角度入手,综合采用药物化学、结构生物学、细胞生物学与实验动物学的研究方法,设计并优化了一系列针对Keap1-Nrf2相互作用抑制剂。
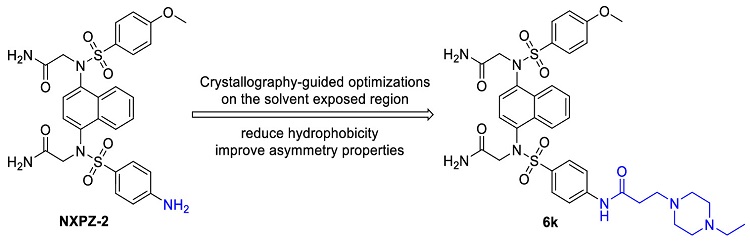
图1. 以结构为基础的药物设计。
在之前的研究中,研究人员已经合成了抑制Keap1−Nrf2相互作用的萘磺酰胺化合物NXPZ-2,但是由于缺乏结构生物学的数据,并不清楚NXPZ-2与Keap1具体的结合方式。此外,由于NXPZ-2的分子结构较为对称,该化合物的溶解性较差,限制了它的临床应用。基于此,研究人员解析了分辨率为2.3 Å的人源Keap1 Kelch domain与NXPZ-2复合体的晶体结构。
通过结构分析,研究人员对复合体结构中NXPZ-2的溶剂暴露区进一步优化,加入了不同的基团,合成了一系列非对称的NXPZ-2衍生物。通过进一步的结构解析,研究人员又获得了3个高分辨的Keap1与NXPZ-2衍生物复合体结构。在这些结构中,衍生物的NXPZ-2骨架与Keap1的结合方式相同,加入基团的电子云较弱,暗示这些基团并不与Keap1稳定结合。药物化学分析发现NXPZ-2衍生物6k表现出了较好的水溶性以及最强的抑制活性。在小鼠模型中,6k 也可以抑制ROS和NO的产生和TNF-α的表达。综上所述,化合物6k可以在脂多糖诱导的急性肺损伤模型(LPS-induced ALI model)中通过提高Nrf2的核转运减少炎症的发生,具有较好的药代动力学特征。提示该类非对称的萘磺酰胺衍生物在Keap1−Nrf2药物设计中的巨大潜力。
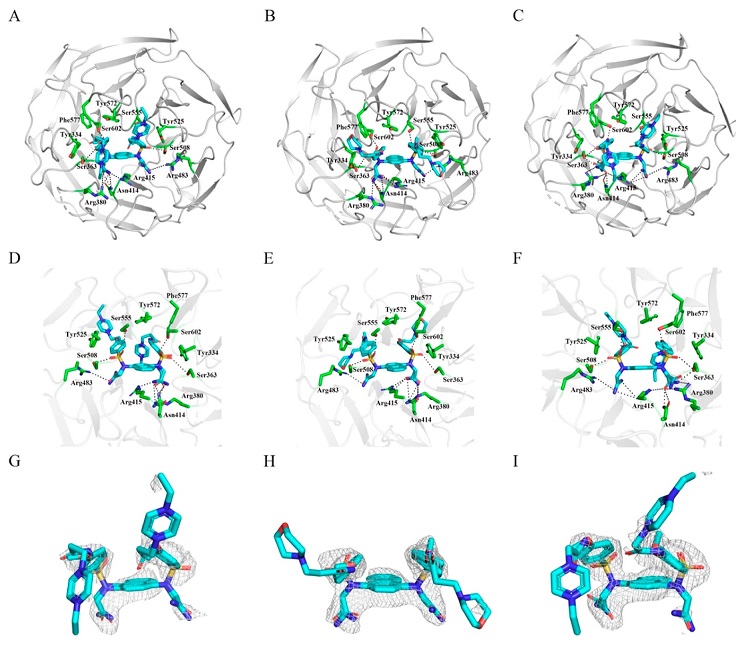
图2. Keap1与NXPZ-2衍生物复合体的结构。
硕士研究生刘国栋、侯瑞林、徐丽娟为文章的共同第一作者,许可教授与庄春林教授为共同通讯作者。该项目获得了科技部、中组部、基金委、上海市科委等基金资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Crystallography-Guided Optimizations of the Keap1–Nrf2 Inhibitors on the Solvent Exposed Region: From Symmetric to Asymmetric Naphthalenesulfonamides
Guodong Liu, Ruilin Hou, Lijuan Xu, Xinqi Zhang, Jianyu Yan, Chengguo Xing, Ke Xu*, and Chunlin Zhuang*
J. Med. Chem., 2022, 65, 8289–8302, DOI: 10.1021/acs.jmedchem.2c00170
许可教授简介

许可,同济大学医学院教授,附属第四人民医院双聘教授,博士生导师。在复旦大学获得生物科学学士学位,中国科学院上海生命科学研究院获得博士学位,美国哥伦比亚大学完成博士后的研究。以第一或通讯作者在国际顶尖学术期刊Nature、eLife、JMC等发表文章多篇,获得国家高层次人才项目资助。课题组聚焦基因转录调控的分子机制和药物研发,常年招收博士后(年薪>30万)、博士硕士研究生。欢迎大家发送邮件到kx2129@tongji.edu.cn报名。
课题组网站:
https://med.tongji.edu.cn/info/1401/7239.htm
https://www.x-mol.com/groups/xu_ke

庄春林,海军军医大学药学院副院长、教授。兼任上海市药学会药物化学专业委员会委员、《Acta Pharmaceutica Sinica B》、《Chinese Chemical Letters》等6本国内外期刊编委。先后入选国家重点研发青年首席科学家,国家“优青”、军队高层次科技创新人才、中国科协青年人才托举工程、上海市曙光学者、上海市晨光学者、上海市卫生系统优秀青年人才等。长期开展创新药物研究工作,在J. Med. Chem.、Chem Rev、Acta Pharm Sin B等国际知名期刊发表论文60余篇,获中国药学会-施维雅青年药物化学奖、全军“优博”、国家海洋科技一等奖等。
