当前位置:
X-MOL 学术
›
Arch. Biochem. Biophys.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
胶束相关的 endomorphin-1 具有结合氧化态铜 Cu(II) 或 Cu(I) 的能力
Archives of Biochemistry and Biophysics ( IF 3.8 ) Pub Date : 2022-05-31 , DOI: 10.1016/j.abb.2022.109305 Yusuke Kuwana 1 , Yuya Ashizawa 1 , Miki Ajima 1 , Takuya Nomura 1 , Mayu Kakeno 1 , Shunya Hirai 1 , Takashi Miura 1

"点击查看英文标题和摘要"
更新日期:2022-06-03
Archives of Biochemistry and Biophysics ( IF 3.8 ) Pub Date : 2022-05-31 , DOI: 10.1016/j.abb.2022.109305 Yusuke Kuwana 1 , Yuya Ashizawa 1 , Miki Ajima 1 , Takuya Nomura 1 , Mayu Kakeno 1 , Shunya Hirai 1 , Takashi Miura 1
Affiliation
|
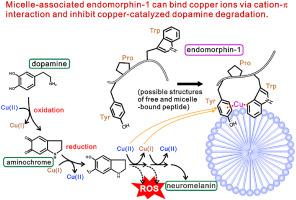
在氧化性细胞外环境中将 Cu(II) 还原为 Cu(I) 是神经退行性疾病的潜在危险因素,因为 Cu(I) 再氧化为 Cu(II) 可以与活性氧的产生耦合。然而,关于如何保护大脑免受铜诱导的氧化应激的影响知之甚少。在本研究中,研究了内源性阿片肽 endomorphin-1 (EM1, Tyr-Pro-Trp-Phe-NH 2 ) 与离子铜的相互作用。EM1 不能用普通的金属配位化学结合铜,因为 EM1 与金属离子的螯合物形成受到第二位的脯氨酸残基的抑制。然而,在存在SDS胶束的情况下,荧光的显着猝灭在添加铜离子时观察到 EM1 的色氨酸侧链,Cu(II) 或 Cu(I)。仅在胶束存在的情况下,将铜添加到 EM1 中也会导致色氨酸的紫外吸收光谱变化,这是阳离子-π 相互作用的诊断。用丙氨酸取代 Tyr1 后,铜诱导的荧光和紫外吸收光谱变化消失. 所得结果表明,EM1通过Tyr1和Trp3芳香侧链的π电子与铜离子结合,它们以胶束缔合形式相互紧密接触。EM1 抑制了将多巴胺转化为神经黑色素的铜催化氧化/还原反应过程,该过程涉及潜在的神经毒性中间体。由于能够结合 Cu(II) 和 Cu(I),EM1 可能具有抑制大脑中铜介导的氧化应激的潜力。目前的结果表明 EM1 的抗氧化作用与其已知的镇痛作用不同。

"点击查看英文标题和摘要"


















































 京公网安备 11010802027423号
京公网安备 11010802027423号