南方医科大学汪枭睿/王晓武教授团队Biomacromolecules | 胆碱聚合物功能化的脂质纳米药物用于肝纤维化治疗
英文原题:Cholinized-Polymer Functionalized Lipid-Based Drug Carriers Facilitate Liver Fibrosis Therapy via Ultrafast Liver-Targeting Delivery

通讯作者:汪枭睿(南方医科大学);王晓武(珠江医院)
作者:Kun Yuan#, Keren Lai#, Guifeng Miao#, Jibin Zhang, Xiaoxi Zhao, Guozhu Tan, Xiaowu Wang*, and Xiaorui Wang*
全球每年有200多万人死于肝脏疾病。各种形式的慢性肝病的进程中往往都伴随着肝纤维化的发生,表现为肝细胞的损伤、肝星状细胞的活化、氧化应激反应的出现和细胞外基质的沉积等,恶化为肝硬化和肝细胞癌的风险急剧增加,最终导致患者死亡。因此,探索有效的肝纤维化治疗策略,在早期抑制甚至逆转肝纤维化,具有极高的临床价值和社会意义。本文研究团队构建了一种新型的胆碱聚合物CP修饰的肝靶向脂质纳米载药平台CP-LNPs,实现纳米颗粒对肝脏的超快靶向,并通过负载具有治疗肝纤维化潜力的药物姜黄素(Cur),显著提升了肝纤维化治疗效果。经静脉注射后,CP-LNPs/Cur在10分钟内就快速富集到肝脏区域,富集效率接近100%,展现出对肝器官的高度特异性。进一步的体内外实验研究表明,CP-LNPs/Cur能够显著地降低肝细胞的氧化应激,减少肝细胞的损伤,同时抑制肝星状细胞的活化,从而有效缓解肝纤维化(图1)。
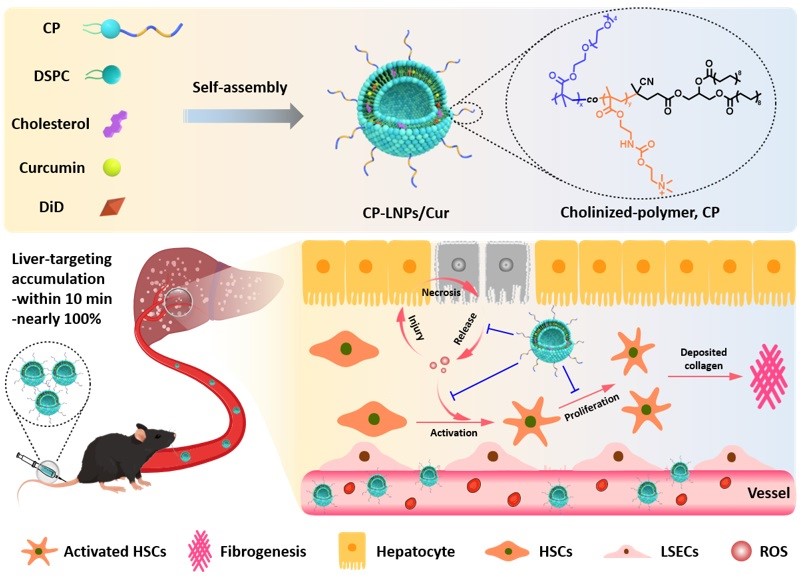
图1. 本文工作概览
作者首先通过RAFT聚合合成了胆碱聚合物(Cholinized-Polymer,CP),并将其和其他脂质分子一同组装为脂质纳米颗粒LNPs。同时,调节CP在LNPs中的不同掺杂比制备不同组成的LNPs,通过小动物活体成像和离体器官成像评估LNPs的肝靶向效果,筛选出肝靶向效果最优的CP-LNP1(图2)。
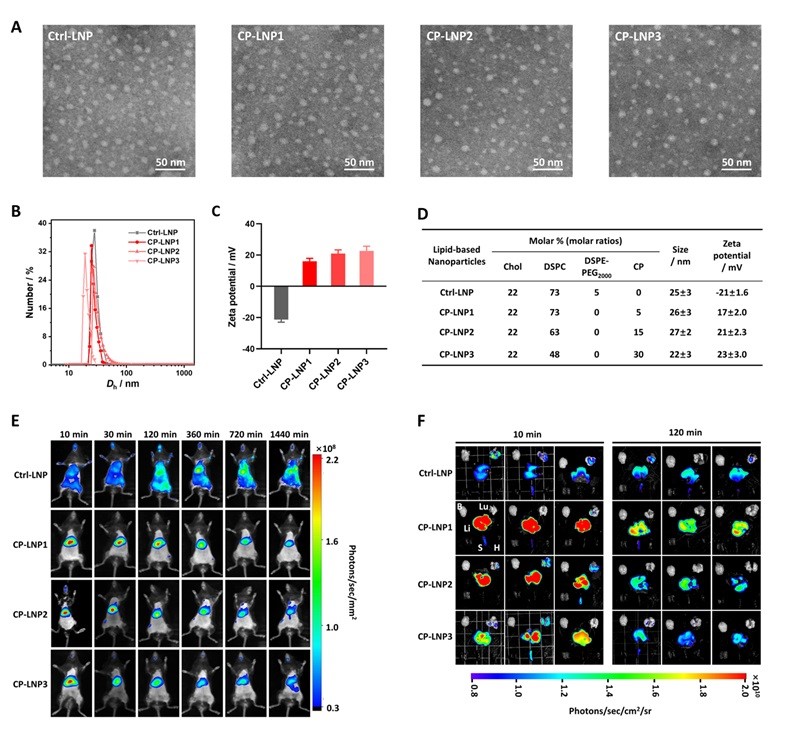
图2. CP-LNPs的结构表征和肝靶向功能筛选
接下来,作者使用最优掺杂比的CP-LNP1负载姜黄素,并通过对比游离姜黄素Cur和对照组脂质纳米颗粒Ctrl-LNP/Cur,评估CP-LNP1/Cur的体外抗纤维化的药效。首先,在确认CP-LNP1/Cur在肝星状细胞LX-2中的摄取增加后,对不同给药处理后LX-2的细胞活力、增殖能力、α-SMA的表达以及迁徙能力进行评估。结果发现,CP-LNP1/Cur显著提升了对肝星状细胞的毒性,更大程度地抑制了活化肝星状细胞的增殖。同时,CP-LNP1/Cur显著下调了LX-2细胞的活化标志物α-SMA的表达,且更有效地抑制了LX-2的迁徙,证明了得益于胆碱聚合物的修饰,CP-LNP1/Cur多方面、强有力地抑制LX-2细胞的活化,为提升肝纤维化的治疗效果打下基础(图3)。
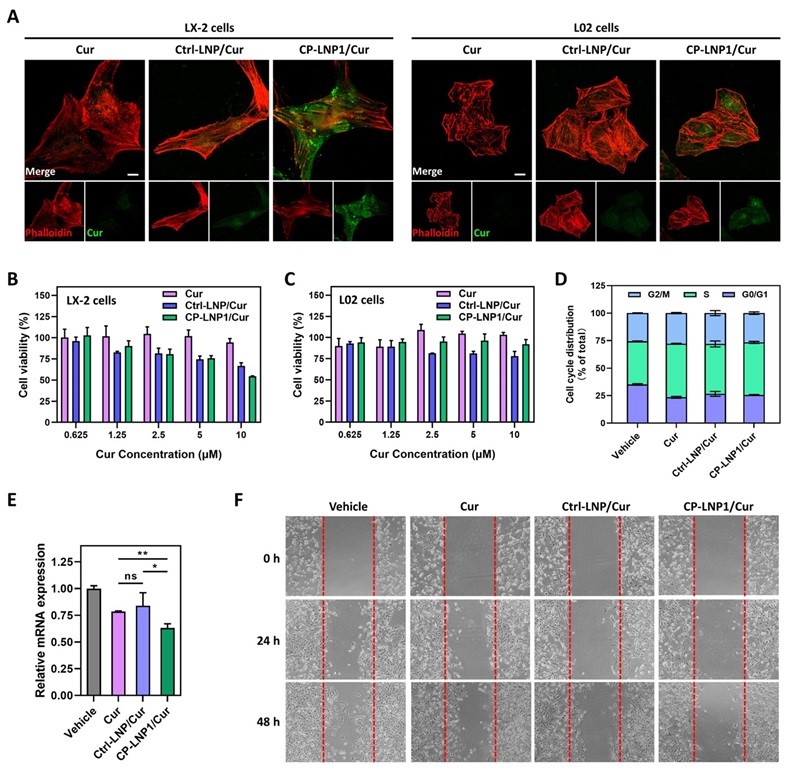
图3. CP-LNP1/Cur体外抗纤维化的药效评估
在肝纤维化的进程中,肝细胞处于氧化应激状态中不断受到损伤。在得知CP-LNP1/Cur在肝细胞L02中的摄取也有增加,且对L02细胞几乎没有毒性的基础上(图3),作者进一步地评估CP-LNP1/Cur对肝细胞的氧化应激保护作用。首先,通过对细胞内的线粒体共定位的分析,发现CP-LNP1/Cur在孵育4 h后与L02细胞的线粒体有较明显的共定位。使用过氧化氢H2O2处理L02细胞模拟肝纤维化情况下的氧化应激状态,分析不同给药处理后的L02细胞的线粒体的膜电位以及细胞GSH的表达情况,作者发现CP-LNP1/Cur更显著地减缓了线粒体膜电位的降低,并且降低了细胞内ROS对GSH的损耗,初步证明CP-LNP1/Cur对肝细胞的保护更为有效。接下来,作者评估了氧化应激条件下不同给药处理对L02细胞的细胞活力以及ROS产生情况的影响,结果表明,CP-LNP1/Cur大大增加了L02细胞的存活率,并减少了ROS的产生。因此,作者提出,经过胆碱的修饰,CP-LNP1/Cur被递送到L02细胞的线粒体后,维持着肝纤维化情况下肝细胞的线粒体功能,并且更为有效地降低氧化应激水平,最终更大程度地保护肝细胞(图4)。
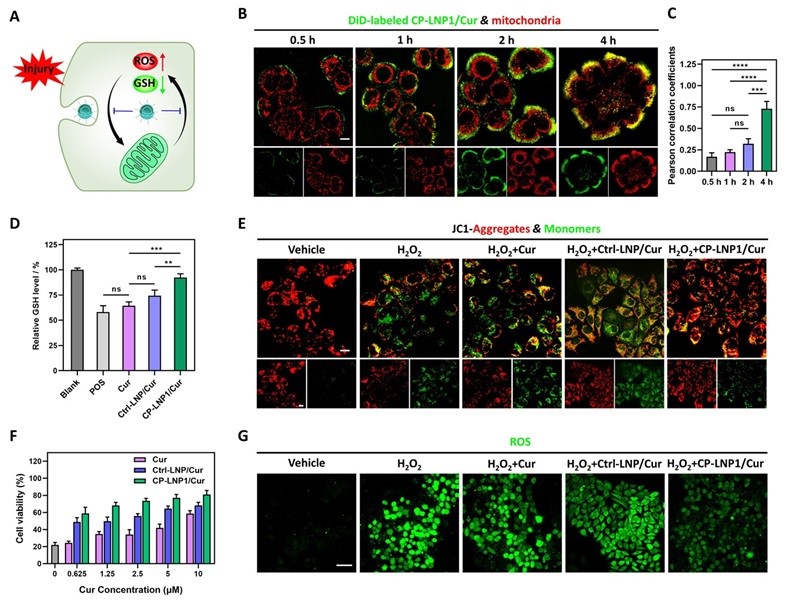
图4. CP-LNP1/Cur对肝细胞氧化应激保护的药效评估
最后,作者评估了CP-LNP1/Cur在CCl4诱导的小鼠肝纤维化模型中的体内药理作用。活体成像数据表明,载药后CP-LNP1/Cur的快速、特异性的肝靶向效果依旧显著,证明CP-LNPs这个载药平台的有效性。在经历四周的CCl4诱导后,对小鼠以姜黄素剂量10 mg/kg进行为期四周给药治疗,每周间隔给药三次。同时,为了排除载体对治疗效果的影响,同样对肝纤维化小鼠分别注射与Ctrl-LNP/Cur和CP-LNP1/Cur的相同载体剂量。对治疗结束后的小鼠肝脏分别进行H&E染色、天狼猩红染色、α-SMA免疫组化分析和ROS免疫组化分析,作者提出,和体外实验的效果一致,相较于其余各组,CP-LNP1/Cur显著地减少了肝脏的脂肪变性,极大程度地减少了肝脏胶原蛋白的沉积,同时降低了α-SMA的表达以及ROS水平,证明CP-LNP1/Cur大幅改善对肝纤维化小鼠的治疗效果。进一步地,通过检测ALT和AST对治疗结束后的小鼠的肝功能进行评估,结果证明CP-LNP1/Cur减轻了肝脏的炎症,一定程度地恢复了小鼠的肝功能。并且,载体对肝纤维化小鼠没有治疗效果,证明治疗效果的提升是由胆碱修饰后的快速靶向后,药物递送效率的提升引起的(图5)。
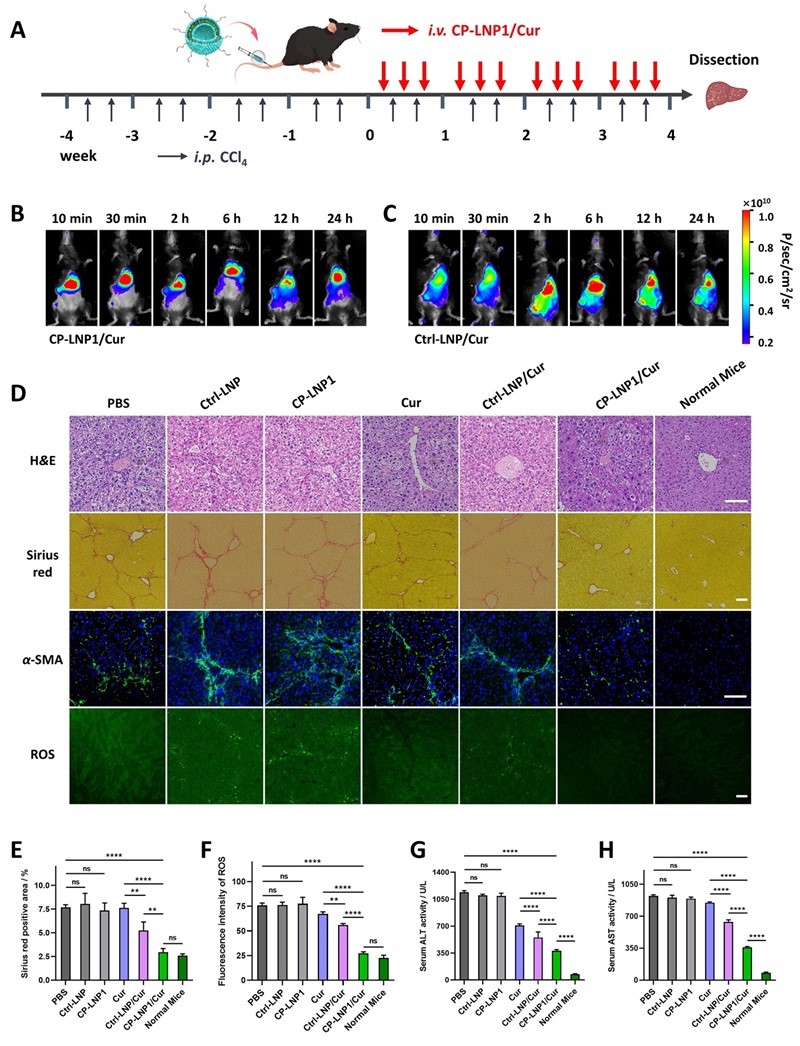
图5. CP-LNP1/Cur对肝纤维化小鼠治疗效果评估
总之,本研究首次提出一种胆碱聚合物修饰的脂质纳米药物递送系统,可以快速地、特异性地靶向肝脏。作为概念验证,通过负载姜黄素证明了这种新型递送系统在肝纤维化治疗中的潜在应用。更重要的是,这种简单而有效的靶向策略,可以进一步拓展肝脏相关疾病的药物递送研究,具有广泛的肝疾病治疗应用前景。该研究论文的第一作者为南方医科大学生物医学工程学院研究生原坤、赖科任与苗贵凤,通讯作者为南方医科大学汪枭睿教授和珠江医院王晓武教授。该研究得到了国家自然科学基金、广东省自然科学基金、广州市科技计划项目及南方医科大学等资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Cholinized-Polymer Functionalized Lipid-Based Drug Carriers Facilitate Liver Fibrosis Therapy via Ultrafast Liver-Targeting Delivery
Kun Yuan, Keren Lai, Guifeng Miao, Jibin Zhang, Xiaoxi Zhao, Guozhu Tan, Xiaowu Wang*, Xiaorui Wang*
Biomacromolecules 2024, XXXX, XXX, XXX-XXX
https://doi.org/10.1021/acs.biomac.4c00691
Published August 30, 2024
© 2024 American Chemical Society
(本稿件来自ACS Publications)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号