远程催化去对称化构建机械平面手性轮烷
轮烷是一类由一个环状分子和一个哑铃状的线型中轴分子相互穿插组成的内锁型超分子结构,该类结构在超分子领域和分子机器领域有着广泛的应用。早在上世纪70年代,化学家已经提出:当大环分子与线型中轴分子都具有旋转不对称性时,即使它们单独都是非手性分子,由其组装而成的轮烷分子仍然会具有手性。该类手性被称为机械平面手性(mechanically planar chirality, MPC),具有这种特殊手性的轮烷被称为MPC轮烷。1977年,第一例光学纯MPC轮烷由Vogtle及合作者通过手性色谱柱拆分得到。近年来,MPC轮烷的手性构筑吸引了越来越多化学家的关注,也为研发手性感应器、分子机器和超分子催化提供了新的视角。
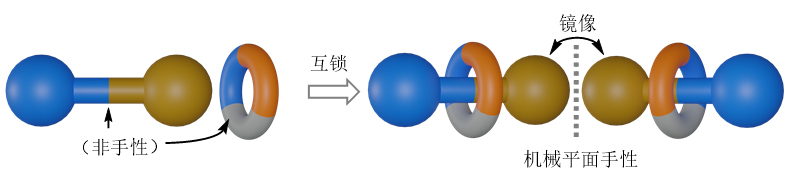
构建具有结构复杂性和官能团多样性的MPC轮烷一直是合成化学的难题。近些年,化学家通过手性辅基、手性互锁辅基、手性试剂控制的动力学拆分三种策略实现了MPC轮烷的合成。然而,现有的方法分别只适用于单一的底物,并且由手性催化剂控制的MPC轮烷的对映选择性合成仍然是该领域的一大挑战。与常见的中心手性和轴手性共价分子相比,轮烷的大环分子与轴分子是通过机械键组合在一起。这种非共价的机械互锁结构中各个组成单元之间的空间关系较为松散,从而为手性催化剂对底物的识别、结合和立体化学调控带来了困难。
新加坡国立大学(NUS)化学系朱烨课题组开发了基于离子键相互作用的手性膦配体,通过钯催化的铃木—宫浦(Suzuki−Miyaura)偶联反应,可对含有季碳中心的前手性底物进行远程催化去对称化(J. Am. Chem. Soc., 2022, 144, 123–129,点击阅读详细)。近期,朱烨课题组联合NUS药学系田冲课题组将该催化体系扩展并成功应用于机械平面手性:手性阴离子膦配体通过离子键与轮烷中轴分子相结合,随后通过铃木—宫浦偶联反应对具有C2v对称性的大环进行去对称化来获得手性富集的MPC轮烷。在这种催化去对称化策略中,机械平面手性的构筑与轮烷分子的组装是分步完成的。因此,该策略同时实现了高效的立体控制和广泛的底物适用范围。
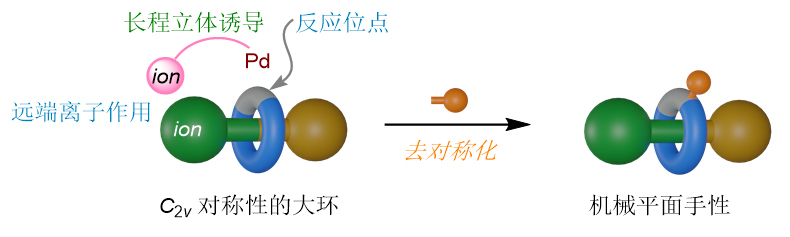
反应设计
科研小组首先研究了前手性的磷酰胺轮烷的催化去对称化反应。这类底物的中轴分子的一个末端芳基带有两个羧基取代基。这两个羧基不仅做为位阻基团帮助实现机械互锁,羧酸根阴离子也可以与离子型的手性催化剂通过正离子桥发生作用,从而实现由离子作用力导向的远程不对称催化。另外,大环分子的氯代芳环作为反应位点参与钯催化的偶联反应。通过这个化学转化,大环分子被赋予旋转不对称性,从而实现由手性催化剂控制的机械平面手性的构筑。
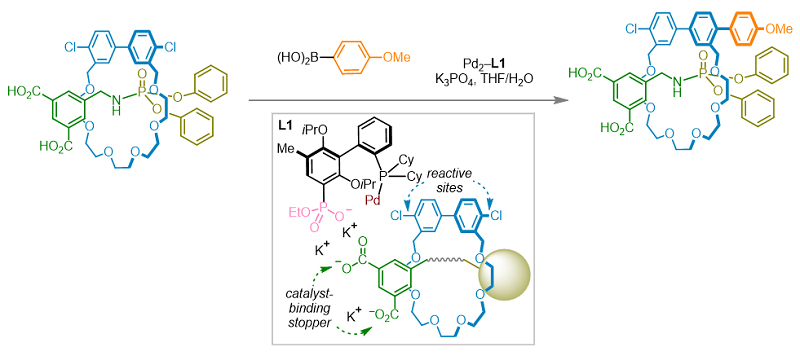
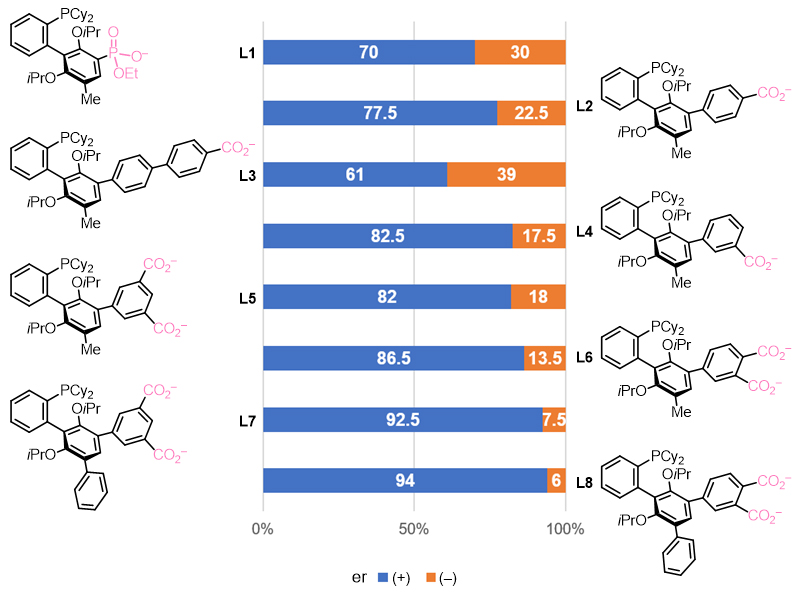
催化剂优化
使用先前发展的带有膦酸负离子的配体L1,产物的对映体选择性达到70比30。这一结果证实了去对称化策略的可行性。为提高立体选择性,科研小组进一步发展了离子手性催化体系。通过在配体的结构中添加一个苯环来增加阴离子和磷原子的距离(L2),对映选择性可以略微提高。当这个距离进一步增加时,对映选择性反而有所降低(L3)。之后通过进一步改变配体中阴离子取代基的位置和数量,科研小组发现双阴离子对于反应选择性有明显的协同效应(L6)。最后,当膦配体中远端取代基的非离子性取代基位阻增大时,去对称化的立体选择性会进一步提高(L8)。
底物扩展
通过对催化体系的进一步优化,多种芳基、杂芳基和烯基硼酸或硼酸酯都可以参与到磷酰胺轮烷的催化去对称化反应。并且,这一反应模式不仅仅局限于磷酰胺轮烷,具有脲或磺胺的前手性轮烷都可以被成功的去对称化。并且,反应不受轮烷轴分子中非离子性的大位阻端基的影响。例如,具有双苯氧基的磷酰胺轮烷和具有二叔丁基苯基或二(三氟甲基)苯基的磺胺轮烷都可以实现高的立体选择性。相对于羧基的位置,磺胺互锁基团的指向对于去对称化反应的选择性没有明显影响。这种催化去对称化反应的广泛的底物适用范围体现了这一新策略相较先前报道的手性轮烷构筑方法的优势。控制实验进一步验证了轮烷中轴分子的羧酸负离子在导向催化剂并实现立体控制中的决定性作用。当使用不可解离的中性轮烷做底物,反应只能得到相对较低的对映选择性。
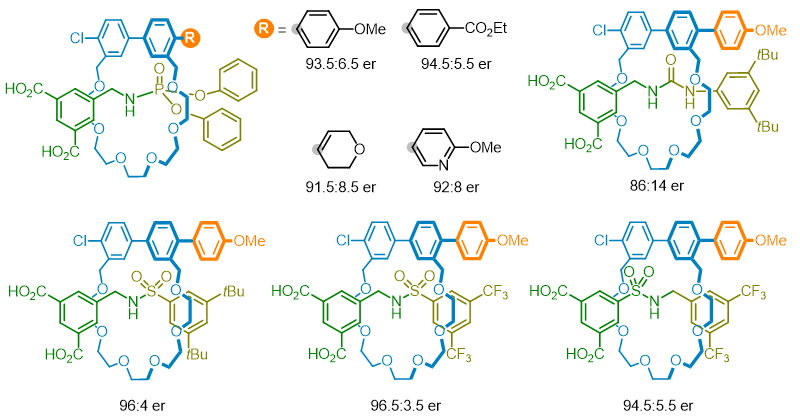
基于非共价相互作用的立体化学控制
轮烷各组分间的互锁关系影响着催化剂与轮烷分子的识别以及机械手性的构筑,而核磁氢谱和单晶衍射则可以探测轮烷组分间的相互作用。
首先,核磁氢谱显示轮烷的亚甲基相较于没有互锁的自由大环分子和自由线型中轴分子中对应的亚甲基都发生了进一步的裂分。比如,轮烷大环上Ho、Hd和轴上的H4都发生了明显的非对映异位裂分。这表明,轮烷的机械立体化学在大环空腔附近得到了很好的表达。再者,大环苯环上的氢(譬如Ha和Hq)以及中轴分子苯环上的氢(H1,H2和H3)化学位移都发生了变化,有可能是两个苯环之间的π-π堆叠引起的。此外,中轴分子上的酰胺键N-H向低场区发生了显著的位移(Δδ = +0.61 ppm),表明其可能与大环上的氧原子存在氢键相互作用。
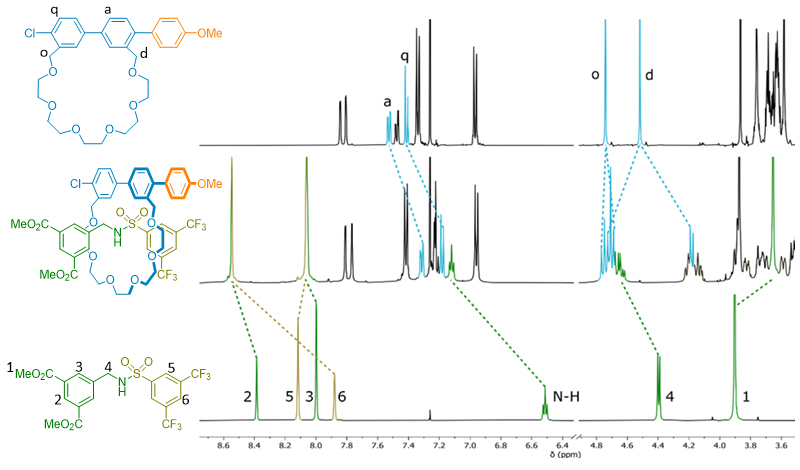
随后,轮烷的单晶X射线衍射结构则更直观的揭示了轮烷组分间的相互作用。单晶结构显示,轮烷分子轴N-H与大环分子拥有最强的氢键相互作用,这一观测与核磁谱图一致。此外,大环的CH与分子轴上磺酰基氧原子也存在氢键相互作用。与此同时,单晶结构显示该类轮烷体系中存在多组π堆积作用。比如,中轴分子的端位苯环上三氟甲基与大环苯环之间的F-π堆积;中轴分子的苯环与大环苯环之间的平行π-π堆积。
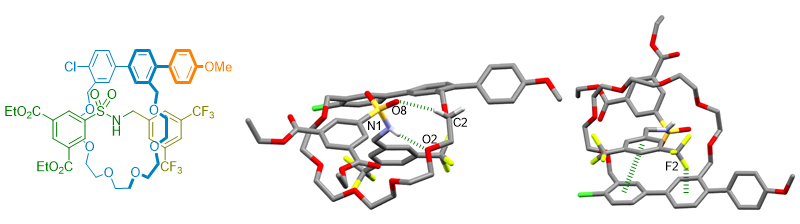
轮烷的组分间相互作用的多样性揭示了机械键构象的多样性,进而影响轮烷-催化剂之间的分子识别以及催化去对称化的立体化学调控。
小结
作者开发了一种由新型催化剂控制的去对称化策略实现了MPC轮烷的高效合成。开发的新型阴离子手性膦配体可以借助轮烷与催化剂之间的端位离子相互作用实现对于机械互锁分子的远程立体化学调控。该策略将MPC轮烷合成中的手性构建和轮烷组装拆分为两个独立的过程,提高了手性构筑的效率,改善了已有策略对于轮烷底物的局限性,丰富了手性轮烷种类。该研究为未来研发新型离子型手性催化剂和机械手性化合物奠定了基础。
这一成果发表在2022年10月出版的Chem 上。文章的第一作者是新加坡国立大学博士后李明凤。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Mechanically planar chiral rotaxanes through catalytic desymmetrization
Mingfeng Li, Xiu Li Chia, Chong Tian, Ye Zhu
Chem, 2022, 8, 2843-2855, DOI: 10.1016/j.chempr.2022.08.009
扫描下方二维码,10月28日前免费查看全文:

通讯作者简介
通讯作者朱烨2012年于芝加哥大学取得博士学位,2012年至2014年在麻省理工学院从事博士后研究,2014年至2018年在百时美施贵宝从事药物研发工作,2018年起就职于新加坡国立大学。研究领域是过渡金属催化剂的发展和在不对称反应中的应用。课题组现有博士后的职位,有意者请联系chmzhu@nus.edu.sg。
https://www.x-mol.com/university/faculty/331622
通讯作者田冲2018年于清华大学取得博士学位,2018年至2021年在曼彻斯特大学从事博士后研究,2021年起就职于新加坡国立大学。研究领域是分子机器和超分子药物。课题组常年诚邀博士生申请,有意者请联系chong21@nus.edu.sg。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号