柠檬苦素(+)-Haperforin G的不对称全合成
柠檬苦素(+)-Haperforin G于2001年首次从越南中部地区的苦木科植物牛筋果中分离得到,2016年,郝小江院士在牛筋果枝叶中将其再次分离提纯。生物活性测试表明,它对人类的11β-羟基类固醇脱氢酶1(11β-HSD1)有明显的抑制作用,IC50可达到0.58 μM,而11β-HSD1是治疗中心性肥胖、代谢紊乱以及心脑血管疾病的新靶点。近日,北京大学化学学院杨震教授和陈家华教授课题组采用高效的汇聚式合成策略,以20步反应、2.0%的总收率完成了(+)-Haperforin G的不对称全合成,为后续的SAR研究,寻找潜在的11β-HSD1的选择性抑制剂提供了可能性。该工作发表在著名学术期刊《美国化学会志》(J. Am. Chem. Soc.)上。
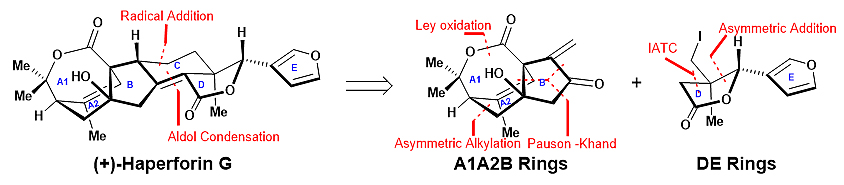
该课题组基于汇聚式的合成策略,选择将分子从C环处断开,使得合成简化为分别构建带有一个季碳手性中心的A1A2B环系和带有一个季碳手性中心的DE环系,然后通过蓝光照射下的自由基加成反应以及分子内羟醛缩合反应构建核心C环,最终完成分子的全合成。
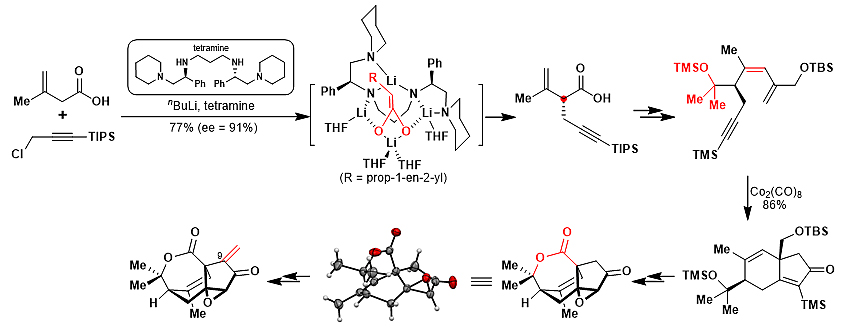
A1A2B环系的合成是以A. Zakarian教授开发的手性四胺类配体介导的直接羧酸α位不对称烷基化反应为起始步骤,以较高的收率及较高的对映选择性引入手性中心。随后经过RCM反应构建三取代的Z式双键,再经由一系列官能团转化得到Pauson-Khand反应前体。值得注意的是,TMS保护的三级羟基以及Z式双键对于Pauson-Khand反应的收率具有重要影响。该Pauson-Khand反应通过半椅式过渡态以大于20:1的非对映选择性构建出含有全碳手性中心的6-5并环。之后通过调整底物构象,经一步Ley氧化完成桥环内酯的构建,该结构经单晶X衍射确认。在此基础上,通过三步反应在大位阻的C9位引入亚甲基,实现了左侧A1A2B环系的构建。
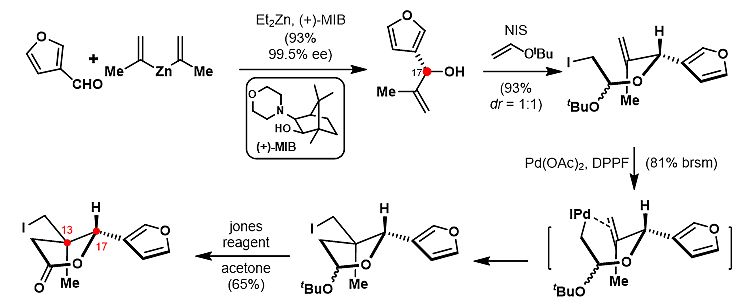
DE环系的合成是以(+)-MIB为手性配体,二异丙烯基锌对3-糠醛不对称加成反应引入手性中心,产物的ee值可达99.5%。随后经NIS介导的缩醛化反应和PdII催化的立体选择性的碘原子转移反应构建出含有C13位全碳手性中心的DE环系。尤为一提的是,该DE环系可以成为汇聚式合成该家族降C16位柠檬苦素的重要中间体。
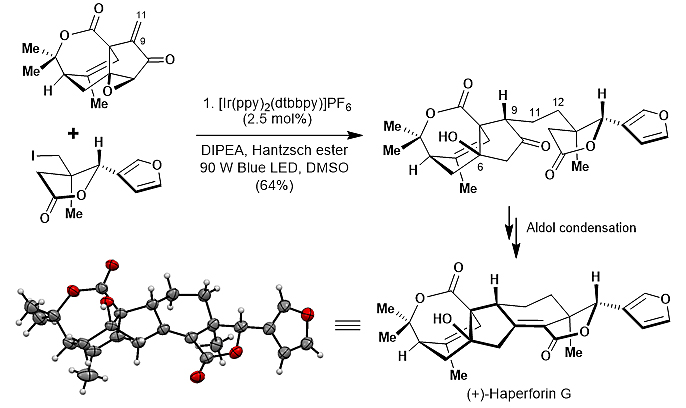
在成功完成两个片段的克级制备之后,通过筛选一系列条件,发现使用[Ir(ppy)2(dtbbpy)]PF6作为催化剂,Hantzsch酯作为有效的氢原子供体,在蓝光照射下,能以64%的收率完成1级烷基自由基参与的分子间Giese反应,成功实现了两个片段的连接,并且同时还原了环氧基团。最后,通过分子内的Aldol缩合反应以及消除反应完成了(+)-Haperforin G的全合成工作,并以单晶X衍射确认了产物结构。
上述高效简洁的合成路线充分展出Pauson-Khand反应在骨架构建及全碳手性中心构建中的独特优势;体现了于环境有利的光反应在全合成应用中的高效性。这条路线的开发对该家族其他天然产物的合成具有指导性意义,为后续SAR研究并找到潜在的11β-HSD1的选择性抑制剂提供了物质基础。相关更为深入的合成研究与化学生物学研究仍在进行之中。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Total Synthesis of (+)-Haperforin G
Wei Zhang, Zhenyu Zhang, Jun-Chen Tang, Jin-Teng Che, Hao-Yu Zhang, Jia-Hua Chen*, Zhen Yang*
J. Am. Chem. Soc., 2020, DOI: 10.1021/jacs.0c10122
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!






















































 京公网安备 11010802027423号
京公网安备 11010802027423号