生物膜主要由脂质和蛋白质组成,呈双分子层的片层结构,厚度约5~10纳米。生物膜既是生理屏障结构,将细胞外环境、细胞质、细胞器内环境隔离,使不同类型的生化反应得以有序和高效地进行;同时,生物膜的结构变化与生理功能及病理过程密切相关。例如细胞膜厚度的变化、溶酶体膜通透性的变化都可激活免疫反应;细胞坏死、细胞焦亡等细胞死亡的过程也常伴随着细胞膜的破损。在纳米生物医学领域,细胞摄入、转运、蓄积、外排纳米颗粒及其在胞内参与的化学反应都与生物膜及其构成的局域环境密切相关。与细胞膜、细胞器膜等作用时,纳米颗粒表面配体的密度、电荷、稳定性、亲疏水性等因素都会影响纳米颗粒在磷脂表面的吸附以及磷脂结构完整性,进而触发炎症反应甚至诱导细胞死亡。例如,聚电解质与表面活性剂是两类配体,被广泛应用于纳米生物医学领域,但其安全性一直存在争议。早期研究认为,纳米表面正电荷是破坏磷脂结构的关键因素;后续研究发现,配体稳定性更为关键,可将表面活性剂分子固化或共价吸附在纳米表面,从而显著降低纳米颗粒对生物膜结构的损伤。但是,纳米颗粒表面配体性质如何调控磷脂结构的分子机制并不清楚,其原因是仍缺乏合适的针对液体界面、高灵敏、高分辨的表征方法,难以定量地解析纳米-配体-磷脂界面的精细结构,也是纳米生物学研究面临的难题和方法学挑战。
针对上述难题,研究组与国家纳米科学中心、芝加哥大学、IBM Watson研究院等团队密切合作,结合同步辐射X射线液体表面散射与分子动力学模拟,建立了液体界面磷脂与纳米颗粒相互作用的定量分析方法,研究了具有不同稳定性、带正电荷配体修饰的纳米颗粒与磷脂作用的界面结构。其中,同步辐射X射线反射反映垂直于界面的电子密度信息,可定量地表征磷脂厚度、吸附角度、磷脂表面的吸附颗粒数;掠入射X射线非镜面散射能够灵敏地表征磷脂表面微量纳米颗粒的吸附;表面等温线测定与分子动力学模拟结合,揭示配体与磷脂分子层作用的过程。研究发现,聚电解质配体修饰的纳米颗粒,配体稳定性强,配体主要通过静电作用吸附在磷脂双层表面,并不改变其结构;表面活性剂配体修饰的纳米颗粒,配体稳定性弱,主要通过范德华力等方式作用于磷脂、插入磷脂双层,导致磷脂异质性、紊乱程度增加,引起磷脂厚度变薄,其效应具有浓度依赖性。当纳米颗粒被巨噬细胞吞噬后,表面活性剂修饰的纳米颗粒导致溶酶体膜通透性增加、激活炎症反应;而聚电解质修饰的纳米颗粒对溶酶体膜结构无明显影响,也未激活炎症反应。细胞水平的结果也验证了配体稳定性对生物膜结构的影响。
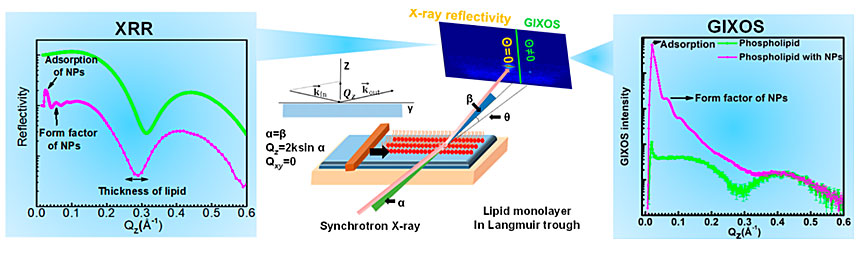
图1. X射线液体界面散射解析纳米颗粒与磷脂作用的界面结构。

图2. X射线液体界面散射与分子动力学模拟结合,揭示表面活性剂、聚电解两类不同稳定性的配体所修饰的纳米颗粒与磷脂分子层相互作用的机制。
该研究建立的液体界面分析方法在纳米生物医学领域有着广泛应用前景和重要意义,既可用于研究纳米材料与生物膜作用导致生物效应的物理化学机制,也能为免疫调节纳米药物、抗菌纳米药物的设计与筛选提供科学依据。
Stability of Ligands on Nanoparticles Regulating the Integrity of Biological Membranes at the Nano–Lipid Interface
Liming Wang, Peiyu Quan, Serena H. Chen, Wei Bu, Yu-Feng Li, Xiaochun Wu, Junguang Wu, Leili Zhang, Yuliang Zhao, Xiaoming Jiang, Binhua Lin, Ruhong Zhou, Chunying Chen
ACS Nano, 2019, 13, 8680-8693, DOI: 10.1021/acsnano.9b00114
论文链接:https://pubs.acs.org/doi/full/10.1021/acsnano.9b00114
