“酶”有话说:Nature Chem.报道分子间苄位不对称C-H键胺化新方法
C-N键广泛存在于活性天然产物、药物分子之中,构建C-N键也成了广大化学工作者研究的重点方向。在诸多构建C-N键的方法中,对有机分子中最广泛存在的C-H键进行胺化,无疑是最为直接、高效的方法之一。然而已有的C-H键胺化策略严重依赖于昂贵的过渡金属,成本高且环境不友好,开发更为绿色的反应体系则显得十分重要。美国加州理工学院的化学家Frances Arnold教授在此领域已经取得了一系列进展,她们开发了酶催化的分子内C-H键胺化反应(J. Am. Chem. Soc., 2014, 136, 15505-15508;Angew. Chem. Int. Ed., 2013, 125, 9479-9482)。相比之下,分子间不对称的C-H键胺化较分子内的反应难度更大,虽然已有一些铑、钌、锰金属催化体系报道,然而迄今为止尚无廉价易得的催化剂能有效实现这一过程。而且,科学家也没有发现有任何一种自然界中的酶可以催化这一反应。
近日,Frances Arnold教授再做突破,她领导的研究团队通过定向进化方法发现了一种基于细胞色素P450单加氧酶(cytochrome P450 monooxygenase)的工程酶,这种包含铁-血红素辅基的工程酶可以高效催化分子间苄位不对称C-H键胺化反应。该工作发表在近期的Nature Chemistry 上,Christopher Prier 和Ruijie Zhang 为共同第一作者。

Frances Arnold教授。图片来源:California Institute of Technology
用酶来催化有机反应并不新鲜,Frances Arnold教授堪称这一领域内的“女神”级人物。她课题组2016年一篇“酶法构建C-Si键”的Science 工作,让不少人惊呼构建“硅基生命”终于成为可能(Science, 2016, 354, 1048-1051,点击阅读详细),这一发现也入选了美国化学会C&EN 评选出的“2016年顶级科研成果”(点击阅读详细)。
Arnold教授团队之前研究分子内C-H键胺化反应的工作,所用的是细胞色素P450单加氧酶的突变体——Arnold教授称其为细胞色素P411。很自然地,Arnold教授团队设想这些细胞色素P411或许可以用于催化分子间C-H键胺化(下图):首先细胞色素P411的血红素辅基被还原为形成二价铁状态1,此后1与TsN3反应形成铁nitrenoid中间体2,2与烷基底物3反应形成C-H键胺化的产物4并重生催化剂1。根据以往的经验,反应中可能存在竞争过程,中间体2会发生降解形成磺酰胺副产物5。以往工作已经证明,细胞色素P411能够高效催化分子内C-H键胺化反应,原因是在分子内反应中,参与反应的C-H键与形成的nitrenoid中间体2距离较近,一定程度上有利于反应进行。然而,在分子间C-H键胺化反应中,底物与nitrenoid中间体2距离较远。因此为了保证C-H键胺化反应顺利进行,nitrenoid中间体2需具有非常高的反应活性,使得分子间C-H键胺化反应的速率高于中间体降解的速率。
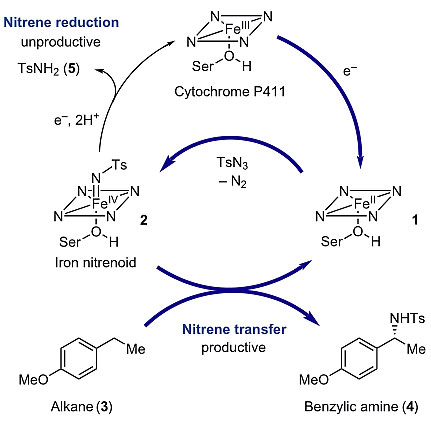
细胞色素P411催化分子间不对称C-H胺化的设想机理。图片来源:Nature Chem.
不过,实际实验结果却不让人满意,几乎所有已知的细胞色素P411——包括那些对分子内C-H键胺化及分子内氮杂环丙烷化反应具有很高催化活性的工程酶,对分子间C-H键胺化都没有任何催化活性,只是生成了相应的磺酰胺副产物。不过事无绝对,她们发现原本设计用于酰亚胺化反应的一种P411突变体——P411BM3 P-4具有微弱的活性,收率11%,e.e. 值14%。随后她们针对P-4进行了定向进化,经过系统的筛选终于发现一种突变体P411CHA(cytochrome P411 C-H aminase)具有最好的催化活性和选择性(下图)。

工程酶的定向进化。图片来源:Nature Chem.
后续的研究中,作者发现P411CHA催化分子间不对称C-H键胺化反应的TON(turnover number)可高达1300,远远高于过渡金属催化分子间不对称C-H键胺化反应的催化效率(目前报道的最高TON为85)。她们随后对P411CHA催化反应进行了进一步的优化,得到最优条件,反应在水中、室温条件下进行,胺化产物4的收率高达86%,对映选择性很好(e.e. > 99%),TON为670(下图)。
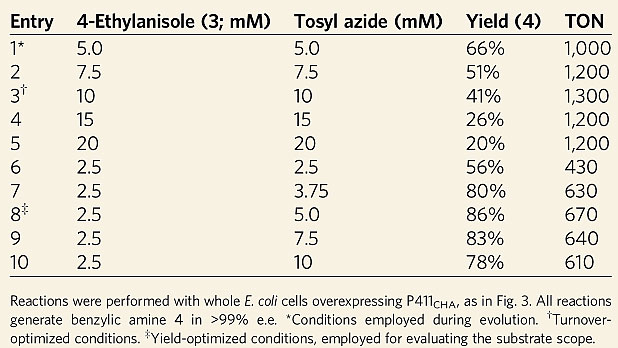
基于P411CHA的反应条件优化。图片来源:Nat. Chem.
接下来是底物适用性研究。下图中已列出大部分可以反应的底物,可以看出,目前该体系具有较大的底物局限性,吸电基团取代的底物产率很低。然而该体系也具有一定的优势,例如产物对映选择性高、TON高等。
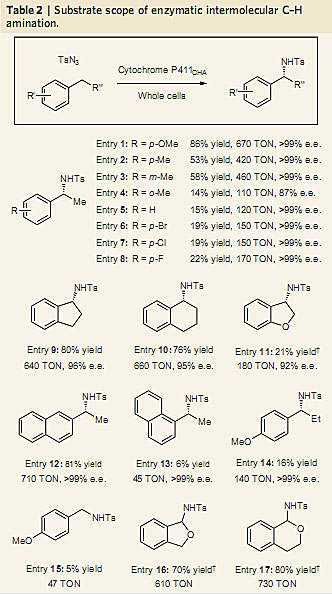
底物适用性研究。图片来源:Nature Chem.
反应对底物的电性非常敏感(富电子底物产率较高),表明该反应中C-H键插入为决速步,氘代实验(下图a,KH/KD = 1.6)进一步验证了这一结论。富电子底物反应产率高有两种可能的原因:(1)相应的酶催化剂具有高C-H键胺化催化活性;(2)相应的酶催化剂一定程度上抑制了nitrenoid中间体降解的副反应。
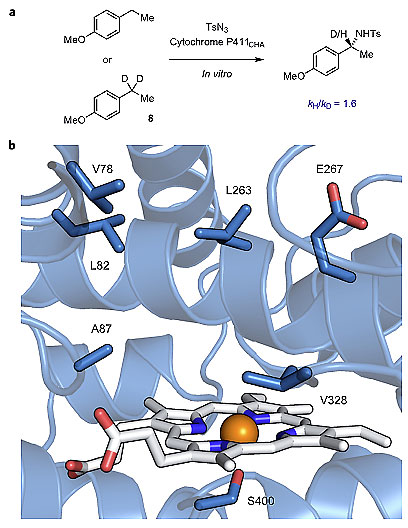
动力学同位素效应的研究以及酶结构的研究(血红素为白色、铁原子为橙色、活性位点氨基酸残基为深蓝色)。图片来源:Nature Chem.
通过对P411CHA酶结构的研究(上图b),她们发现P411CHA具有高效催化活性的原因在于酶较好地调节了活性氮物种与烷烃底物的交互作用,P411CHA具有合适的血红素远端口袋体积,底物通过范德华力与A87、L263、E267和V328等相结合,使得C-H键与氮宾距离较近,从而使分子间C-H键胺化反应得以高效进行。
——总结——
Frances Arnold教授课题组发现一种包含铁-血红素辅基的工程酶——细胞色素P411CHA对分子间苄位不对称C-H键胺化反应具有高度的催化活性。尽管底物适用范围有限,但反应具有非常明显的优点,即产物的对映选择性高、TON高。另外,这种工程酶还有望用于更多目前化学催化不能实现的C-H键官能团化反应。通过对现有酶催化剂进行改进,人们有望解决一些传统合成化学的难题,甚至挑战目前化学催化无法实现的化学转化。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Enantioselective, intermolecular benzylic C–H amination catalysed by an engineered iron-haem enzyms
Nature Chem., 2017, DOI: 10.1038/NCHEM.2783
(本文由Chem-Stone供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
《Nature》:血红素换个“心”,催化大不同 2016-06-23
-
Science:首例蛋白质催化C-Si键的形成,将C-Si键引入生命体成为可能 2016-12-17
-
聊一聊Sukbok Chang的C-H键胺化新进展 2017-03-15
-
细胞色素P450催化的真菌天然产物的区域和立体选择性酚偶联 2015-09-25
































 京公网安备 11010802027423号
京公网安备 11010802027423号