小小海螺,开启止痛药大变革
阿片类(opioids)止痛药是目前临床治疗中度至重度急性疼痛和癌症疼痛的一线药物。但是,这类药可以说是毁誉参半。根据美国疾控中心(CDC)数据[1],仅2015年就有超过15,000人因阿片类处方药物的过量使用而死亡。由于阿片类的严重副作用和高度成瘾性,而且对慢性疼痛是否有效还存有争议(去年一项研究表明阿片类药物甚至会加重慢性疼痛,点击阅读详细),科学家正努力寻找代替现有阿片类的新一代止痛药。近年来,科学家们的努力取得了一些进展,比较有代表性的比如去年Nature 报道的一种无副作用的阿片受体靶向药物(点击阅读详细)。
最近,犹他大学(University of Utah)Baldomera M. Olivera和J. Michael McIntosh等科学家发现一种小小的海螺可以分泌一种有效的止痛物质,它能代替阿片类止痛药的药效,不过经历的信号通路却完全不同,因此没有阿片类的成瘾风险。而且,啮齿动物实验表明这种新物质的效力时间很长。这项成果发表在最近的《美国科学院院刊》上。

Baldomera M. Olivera教授和J. Michael McIntosh教授。图片来源:University of Utah
与不少人选择合成化合物或者修饰已有化合物结构不同,Olivera在止痛药物研究领域有自己的思路。他认为:“自然界已经创造出了足够复杂多样的分子,隐藏着意想不到的用处。” Olivera实验室擅长用自然界的各种毒液来理解神经系统的不同信号通路。这一次的突破也是来自小小的“危险份子”—— 一种芋螺属海螺,学名Conus regius。这种外壳华丽造型浮夸的软体动物实际上比看上去危险得多,长着注射器一样的“毒牙”,分泌的毒液能使猎物瘫痪并死亡。

芋螺准备捕获小鱼。图片来自网络
研究人员发现这种海螺的毒液中有一种名为RgIA的肽类化合物,能够作用在一条非阿片类靶点的疼痛通路。在啮齿动物模型中,研究者证明了α9α10烟碱乙酰胆碱受体(nAChRs)是这条疼痛通路的受体,也是RgIA的靶标。

RglA的肽链及突变的残基位点。图片来源:PNAS
研究者以RgIA为起点,对甘氨酸和半胱氨酸以外的残基做了精细地突变,总结了不同残基对活性的影响,制备了一系列RgIA类似物。其中RgIA5(IC50 = 0.44 nM)的活性最高,RgIA4(IC50 =1.5 nM)次之,但后者在不同受体间的选择性更好,因此研究者最终选择RgIA4作为先导化合物。
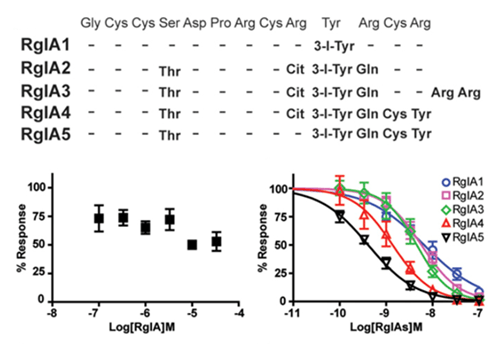
五条RgIA类似物的肽链及对人类α9α10 nAChR的抑制活性,其中RgIA5的活性最强。图片来源:PNAS
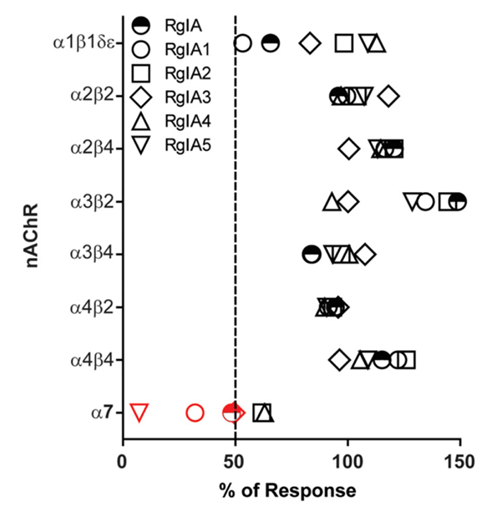
RgIA5对α7 nAChR的抑制活性也非常强,说明其特异性不佳。而RgIA4则是该系列分子中特异性最好的。图片来源:PNAS
要知道,阿片类以外的疼痛疗法非常少见,这项研究无疑具有开拓性。
为了检测这些分子的止痛能力,研究者用化疗药物使一些小鼠对疼痛变得极为敏感,简单的触碰也会使这些小鼠变得非常激动。注射了RgIA4的小鼠则不会那么痛苦,而敲除了α9α10烟碱乙酰胆碱受体的小鼠也不会感到疼痛。这些实验有力地证明α9α10烟碱乙酰胆碱受体是疼痛受体,而RgIA4可以抑制其激活。
不过这个分子的神奇之处还不仅如此,当它从动物的血液中消失之后,止痛的效果却还能持续很长时间。实验证明,RgIA4分子在注射入动物体内4小时后就完全降解,但药效却长达72小时以上!这似乎暗示着RgIA4除了止痛,还对神经系统有修复功能。
这些结果预示着这个分子有预防疼痛的能力。一直以来,医生对慢性疼痛都束手无策,这种化合物则可能是一种有潜力的治疗方法。
寻找安全的止痛药和治疗慢性疼痛一直是医学界的两大难题。这种取自海螺毒液,经过人类稍加改造的分子为解决这两个难题都带来了希望。另外,由于RgIA4本身是多肽分子,找到高效廉价的生物合成方法应该并不是难事。
正如Olivera教授所说,很多问题的答案,大自然早已准备好,就等着人类去发现了。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Inhibition of α9α10 nicotinic acetylcholine receptors prevents chemotherapy-induced neuropathic pain
PNAS, 2017, DOI: 10.1073/pnas.1621433114
参考资料:
1. https://www.cdc.gov/drugoverdose/data/overdose.html
2. https://phys.org/news/2017-02-alternative-opioids-compound-marine-snail.html
(本文由氘氘斋供稿)
