PARP抑制剂:给癌细胞下个套
除了如紫外线辐射等外界因素会对DNA造成损伤之外,DNA分子自身的不稳定性以及细胞分裂时DNA复制产生的错误,都可能让基因组变得一团糟。但是,我们的基因并没有如此,其中最大的功臣就是DNA损伤修复机制,2015年,在这个领域内做出卓越贡献的三位科学家也获得了诺贝尔化学奖。
目前,放疗和很多抗肿瘤药物通过损伤肿瘤细胞的DNA来达到杀灭肿瘤细胞的效果,但肿瘤细胞也不会坐以待毙,它们够激活DNA损伤修复机制来进行修复,从而导致对此类抗癌疗法的抗性。在肿瘤细胞中确实能够检测到DNA修复酶的过度表达,因此阻断DNA修复通路是肿瘤治疗的一种重要途径。
今年是Chambon等人发现聚(ADP-核糖)聚合物(poly(ADP-ribose) polymer,PAR)50周年,形成聚(ADP-核糖)聚合物(也称“PAR化”,PARylation)是首个被详细描述的与DNA损伤和修复以及染色质重塑相关的翻译后修饰过程。一年之后,第一个PAR聚合酶PARP1被发现。PARPs在DNA损伤修复中发挥着重要功能,而PARP抑制剂也是首个获准上市的靶向DNA损伤修复机制的抗癌药物。最近,美国NIH国家癌症研究所的Yves Pommier等在Science Translational Medicine上撰写评述性文章,介绍了PARP抑制剂的作用机制和进展。(把PARP看成PPAP的,请自觉面壁5分钟且脑子里不能出现小胡子男的形象……)
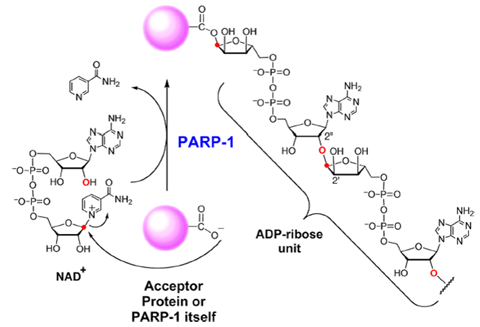
图1. PARP1的催化反应。图片来源:Biochemistry, 2014, 53, 1779-1788
▌PARPs的DNA修复作用
在参与DNA修复的众多酶中,PARPs起到了重要作用,这个家族包括17种酶,具有ADP-核糖转移酶活性。PARP1和PARP2能修复DNA单链断裂(SSBs),PARP1还能修复DNA双链断裂(DSBs)以及复制叉损伤(图2)。PARP1作为DNA断裂的感受器,在DNA损伤后被激活,识别并结合到DNA断裂部位,减少重组发生并避免受损DNA受到核酸外切酶的作用。在与DNA缺口结合后,通过自身的糖基化来催化烟酰胺腺嘌呤二核苷酸(NAD+)分解为烟酰胺和ADP核糖,再以ADP核糖为底物,使受体蛋白以及PARP1自身发生“PAR化”,形成PARP-ADP核糖支链(图1),一方面可防止附近的DNA分子与损伤的DNA进行重组;另一方面能够吸引DNA修复蛋白结合并降低PARP1与DNA的亲和性,使PARP1从DNA断裂处解离,然后DNA修复蛋白与DNA缺口结合,对损伤部位进行修复。而PARP1的“PAR化”会被其他酶清除,使得PARP1恢复活性,寻找下一个DNA断裂(图2)。
PARP1和PARP2的功能有重叠,不过可能对底物的选择性并不相同。实验证明,如果敲除PARP1和PARP2中的一个,小鼠还能成活,但两个同时敲除却是致命的,细胞的基因组变得很不稳定。目前临床上使用的PARP抑制剂,都能同时抑制PARP1和PARP2,这或许说明了药理学的活性抑制与基因手段的蛋白缺失,效果并不相同。
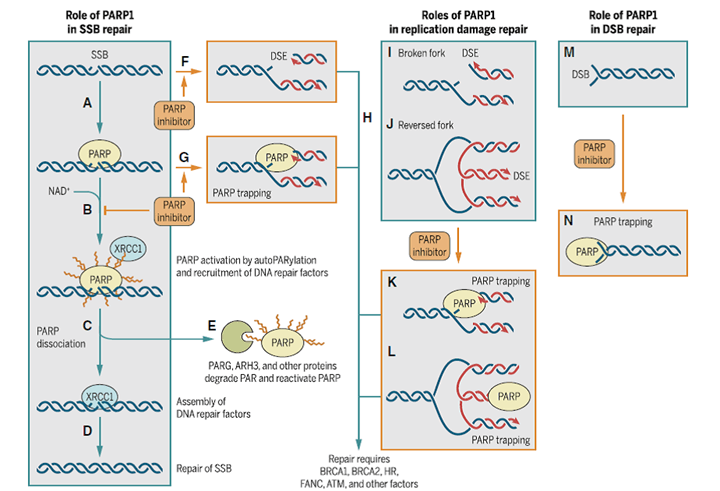
图2. PARP1修复DNA以及PARP抑制剂的作用。图片来源:Sci. Transl. Med.
▌PARP抑制剂的作用机制
最初认为,PARP抑制剂使DNA单链断裂未能正常修复,从而在细胞中变成遗传毒性更强的单端双链断裂(single-ended double-strand break,DSE)(图2 F)。不过,在正常细胞中,DSE损伤会激活细胞内DNA损伤应答,启动同源重组修复(HRR)机制进行有效修复(图2 G),但缺乏这种机制的肿瘤细胞,例如发生BRCA功能缺失突变,基因组的不稳定性加剧,最终导致肿瘤特异性的细胞死亡。
对BRCA突变的肿瘤细胞来说,单独的PARP抑制或BRCA缺失都不致命,但两者合在一起就会导致细胞死亡。这种协同致死(synthetic lethality)效应,也就是临床单独应用PARP抑制剂作为治疗方案的基础。
PARP抑制剂能够结合到PARP1(和/或PARP2)的NAD+结合口袋,造成构象异构,稳定了DNA-PARP的可逆解离,使PARP保持对DNA的结合,这个过程被称为DNA-PARP复合物的“捕获(trapping)”,这导致DNA-PARP复合物长期存在,无法进行后续的修复(J. Med. Chem., 2016, 59, 9575-9598)。相比较而言,PARP抑制剂造成PARP捕获的伤害要高于单纯抑制PARP的催化活性。
PARP抑制剂造成的PARP捕获,或许能够用于解释为什么PARP抑制剂造成的细胞毒性要远高于敲除PARP1造成的细胞毒性,以及为什么敲除PARP1基因反而会抵消PARP抑制剂造成的细胞毒性。
PARP抑制剂的这种捕获作用机制其实并不罕见,至少有三类抗药物的作用机制与之类似,包括:拓扑异构酶I(TOP1)抑制剂、拓扑异构酶II(TOP2α和TOP2β)抑制剂以及DNA甲基转移酶(DNMT)抑制剂。它们的细胞毒活性既与酶催化抑制有关,又与捕获靶标的DNA-蛋白复合物有关。
▌基于捕获作用的PARP抑制剂结构
PARP1的天然底物为NAD+,目前已有的PARP抑制剂大多模拟NAD+中的烟酰胺结构,作用于PARP1的活性位点而发挥抑制活性。单独使用PARP抑制剂的细胞毒性并不和它们抑制“PAR化”的能力(也就是酶的催化活性)成正比。现在临床上使用的PARP抑制剂基本都是催化抑制剂,它们捕获DNA-PARP复合物的能力不同,按照捕获能力大小依次为:talazoparib >> niraparib > olaparib = rucaparib >> veliparib,这个排名也与它们细胞毒性的排名相同。Veliparib在100 μM时对大多数癌细胞都无效,而talazoparib的有效浓度仅为nM级别。这些抑制剂的结构大小和柔性大不相同:veliparib最小,分子量为244,而olaparib的分子量达434;talazoparib最显刚性,含有两个对抑制PARP至关重要的手性中心。Talazoparib的立体特异性以及较大的结构,或许是它PARP1和PRAP2捕获活性超高的原因(图3)。

图3. PARP抑制剂的结构(通用的烟酰胺部分用酒红色显示)。图片来源:Sci. Transl. Med.
▌PARP抑制剂的抗药性以及与其他化疗药物的联用
与PARP捕获有关的临床结论是,药物的抗癌效果依赖PARP1的水平,PARP1越多,造成PARP捕获的机会越多。因此,一种抗药性机制就是下调PARP1的表达。另一种抗药性机制与药物外排泵有关,有些PARP抑制剂是药物外排泵的底物,如olaparib和rucaparib是MDR1的底物。另外,同源重组修复缺失(HRD)也是PARP抑制剂效果好坏的决定因素,一些BRCA缺失的肿瘤会再次激活同源重组修复功能,从而使PARP抑制剂的治疗效果一落千丈。
与PARP抑制剂能产生协同效应的联用化疗药物包括DNA烷化剂temozolomide和TOP1抑制剂(例如irinotecan和topotecan)。
▌PARP抑制剂的临床剂量
PARP抑制剂的作用机制带来另一个问题,强大的PARP捕获能力怎样转化为临床抗癌活性?尽管单独比较PARP的活性较难,但越来越多的数据说明PARP抑制剂的PARP捕获能力与其抗癌活性可能不是简单的相关而已。尽管PARP捕获能力越强,PARP抑制剂的临床效果会越好,但对正常组织的毒性也越大。例如,talazoparib捕获PARP的能力比niraparib、rucaparib和olaparib高2-3个数量级,但它的毒性也很大,二期临床数据证明它的推荐剂量要比后者低300至1200倍。
—— 结语 ——
从发现PARP1到临床批准第一个以此为靶标的药物,间隔了50年的时间。现在PARP抑制剂已成为治疗BRCA突变高分级浆液性卵巢癌的标准方法,也有希望用于前列腺癌和乳腺癌某些亚型的治疗。PARP在DNA修复中起到多重作用,理解PARP抑制剂的作用机制非常重要,特别是PARP捕获。对药物作用机制的了解是很多过程的基础,诸如选择药物的适用患者人群,决定给药剂量和治疗方案,以及了解药物抗性产生的原理。
原文(扫描或长按二维码,识别后直达原文页面):

http://stm.sciencemag.org/content/8/362/362ps17
Laying a trap to kill cancer cells: PARP inhibitors and their mechanisms of action
Sci. Transl. Med., 2016, 8, 362ps17, DOI: 10.1126/scitranslmed.aaf9246
