具有靶向和荧光成像功能的碳点实现脑肿瘤诊断
在区分肿瘤细胞与正常细胞实现肿瘤的早期诊断过程中,靶向分子起着至关重要的作用。通常采用将靶向试剂通过化学键连接到具有成像功能的聚合物胶束或纳米颗粒的外表面,形成具有多功能制剂。然而,多步的化学反应使得成像或者靶向功能弱化。因此发展多功能(靶向、成像和治疗)的制剂对于纳米药物和个性化治疗的发展有着重要的意义。
碳点(Carbon Dots)具有优异的发光特性、良好的生物相容性、低毒性、强亲水性和表面易功能化等特性,以碳点为荧光制剂并赋予其更多的功能,将进一步开拓其在生物相关的应用,且具有使用的价值。为其在生物医学等领域的广泛应用提供了得天独厚的有利条件。中国科学院的孙再成研究员,谢志刚研究员和郑敏副研究员的合作研究团队首先利用碳点作为药物载体,通过与抗肿瘤药物的共价偶联成功地制备出新型的集荧光成像和肿瘤治疗于一体的诊断治疗纳米药物(Adv. Mater.2014, 26, 3554–3560)。然而,该纳米药物体系仍然面临着药物利用度低,肿瘤靶向性差、系统毒性强等关键科学问题。为了提高药物的生物利用度,降低对正常组织和细胞的毒副作用,可以在抗肿瘤药物的载体上引入靶向试剂,通过靶向作用将药物定向输送到病灶部位。但是,构建具有靶向,成像和治疗等多重功能的智能化纳米药物仍然面临着巨大的挑战。
该团队在前期工作的基础上,利用一步法开发出具有靶向功能的碳点,此类碳点具有卓越的多色发光特性,有助于实现体外的细胞成像和活体内更深层组织的荧光成像。更重要的是,此碳点在不需要额外的引入靶向分子的情况下,即可实现对脑肿瘤细胞的高度选择性。合作单位四川大学的高会乐副教授课题组通过荧光活体成像系统观察碳点在荷瘤小鼠内的生物分布。从小鼠的活体成像数据来看,通过尾静脉注射的碳点能在5分钟内快速地穿过血脑屏障,并选择性地富集在脑胶质瘤内,而在正常脑组织内的分布却非常少,充分证实了碳点对脑胶质瘤的靶向成像功能,为脑肿瘤的早期诊断和进一步地构建智能化纳米药物奠定了坚实的基础。
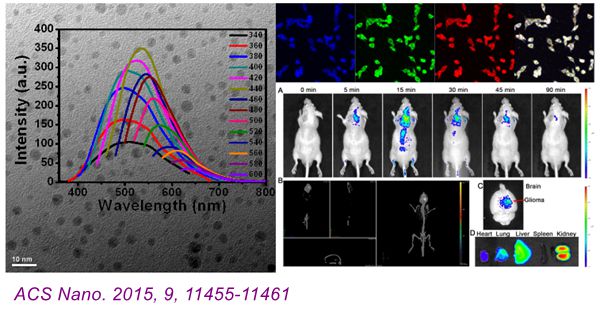
相关研究成果发表在国际知名期刊《ACS Nano》上(ACS Nano.2015, 9, 11455-11461)。
http://pubs.acs.org/doi/abs/10.1021/acsnano.5b05575
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号