借助近红外比率型荧光探针成像分析CS2胁迫下细胞内硒醇浓度变化
硒有利于保护机体对抗炎症和促进免疫系统功能,其生理功能在很大程度上取决于含硒氨基酸和硒蛋白。硒代半胱氨酸(Sec)能调节甲状腺代谢,维持细胞的氧化还原状态并保护细胞免受氧化损伤。因此,Sec被认为是抗氧化应激的一线抗氧化防御系统,在保护机体免受氧化损伤和修复氧化剂对脂质、蛋白质或DNA的破坏方面起着重要作用。
CS2是一种广泛的具有细胞毒作用的酶抑制剂,可以破坏细胞的正常代谢并干扰细胞信号转导。CS2可与氧化还原酶的关键活性部位如硒醇基(-SeH)反应。氧化还原酶的抑制会阻碍细胞内氧化还原平衡,并异常增加活性氧物质的水平。过量产生的活性氧物质可攻击生物膜中的不饱和脂肪酸并引发自由基链式反应,诱导细胞器的氧化损伤并引起相关疾病,这些氧化还原酶大部分存在于线粒体中。目前,线粒体中CS2中毒的发病机制尚不清楚。因此,有必要进一步研究CS2在线粒体中的毒理作用。考虑到CS2与Sec之间的潜在关系,我们推测可用Sec作生物标志物来评估CS2胁迫下活细胞和活体中的氧化还原水平波动情况。
常用的定量检测Sec的方法包括高效液相色谱法、核磁共振波谱法和耦合等离子体质谱法。虽然这些方法可以精确检测Sec的浓度,但它们通常需要复杂的样品预处理且无法实现实时和原位检测。与这些检测技术相比,基于荧光探针的荧光成像技术已广泛用于生物活性物种的荧光成像分析,得益于其高灵敏度、高选择性、低侵入性、快速响应以及高空间和时间分辨率等优点。然而,到目前为止,还没有近红外比率型荧光探针用于靶向线粒体,检测二硫化碳胁迫下急/慢性肝炎爆发过程中Sec的浓度变化。
海南医学院功能材料与分子影像研究所与中科院烟台海岸带研究所合作设计合成了一种近红外比率型荧光探针(Mito-di NO2),用于在线粒体相关炎症和急/慢性肝炎期间Sec浓度变化的定量分析。探针由三部分组成:近红外七甲川花菁荧光团、2,4-二硝基苯磺酰胺响应基团和亲脂性三苯基膦阳离子线粒体靶向基团。
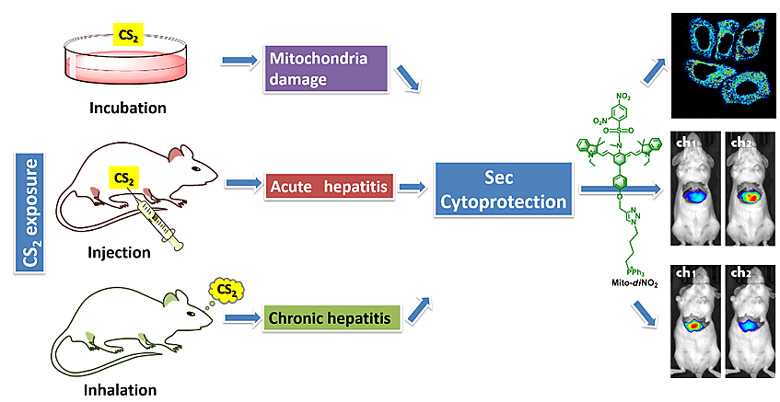
该近红外比率型荧光探针具有线粒体靶向功能,可用于选择性和灵敏地检测CS2刺激下细胞和小鼠模型中Sec的浓度变化。在0-7 μM Sec浓度范围,探针的比率荧光强度的对数值和Sec浓度之间存在良好的线性关系(r = 0.9921),检测限为40 nM。Mito-di NO2对Sec的荧光响应可在4分钟内快速完成且不受其它活性硫物种的干扰。该探针定位到线粒体,并检测各细胞系中内源性Sec的浓度;在CS2暴露下引起的线粒体相关的急性炎症中,该探针可检测Sec浓度和细胞炎症之间的关系;在CS2暴露下诱导的小鼠急性和慢性肝炎模型中,该探针可分析Sec在肝脏中的保护作用并评估CS2中毒期间肝脏损伤的程度。实验结果表明,Sec可以保护细胞免受炎症损伤。利我们希望探针Mito-di NO2不仅可以作为CS2胁迫下机体炎症准确诊断和治疗工具,而且可以揭示化学污染和生理健康之间的关系。
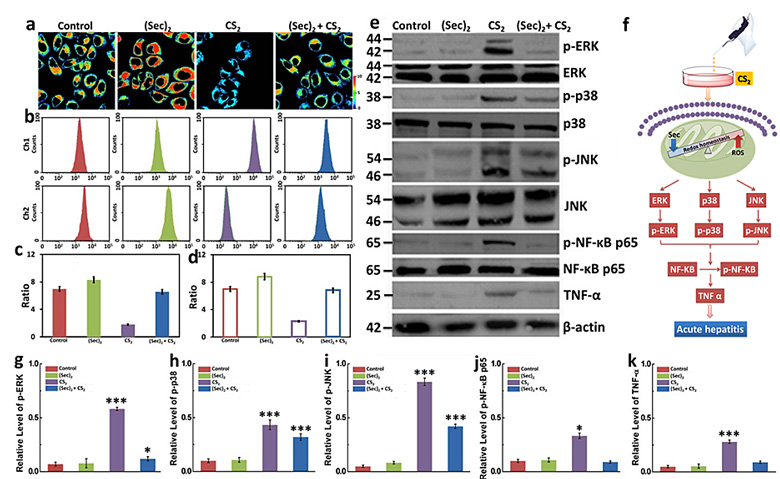
评估Sec在CS2诱导的线粒体相关炎症过程中的保护作用和CS2诱导的线粒体相关的炎症信号通路。活细胞中Sec的产生能保护细胞免受炎症损伤。
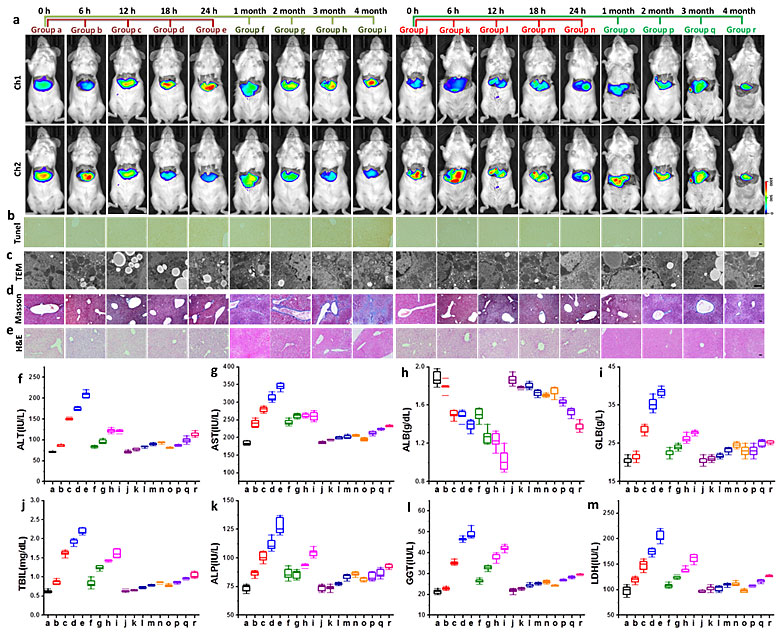
探针评估小鼠急/慢性肝炎模型和治疗模型中的硒醇浓度。病理结果表明,CS2短期高剂量暴露导致严重急性肝炎,而长期吸入CS2导致慢性肝炎。治疗组的结果说明Sec可以有效降低由CS2引起的细胞毒性和肝组织损伤。在急性炎症阶段,Sec浓度在6小时内先增加后降低,这可能是面临急性肝炎时机体的自我保护作用。与急性肝炎组不同,慢性肝炎组Sec浓度持续下降。治疗组中相对稳定的比率信号表明Sec的浓度已经得到有效补充。
这一成果近期发表在Analytical Chemistry 上,文章的第一作者是中国科学院烟台海岸带研究所博士研究生韩潇玥(现为牛津大学博士后)。通讯作者为于法标教授和陈令新研究员。
该论文作者为:Xiaoyue Han, Rui Wang, Xinyu Song, Fabiao Yu*, and Lingxin Chen*
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Evaluation Selenocysteine Protective Effect in Carbon Disulfide Induced Hepatitis with a Mitochondrial Targeting Ratiometric Near-Infrared Fluorescent Probe
Anal. Chem., 2018, 90, 8108–8115, DOI: 10.1021/acs.analchem.8b01306
于法标博士简介

于法标,海南医学院功能材料与分子影像研究所教授。2013年于大连理工大学/中国科学院大连物理化学研究所取得博士学位。2013年8月至2017年9月在中国科学院烟台海岸带研究所工作,2017年10月起就职于海南医学院。
功能材料和分子影像研究所(Institute of Functional Materials and Molecular Imaging, Hainan Medical University)依托海南医学院(海南热带医科大学)。负责人为于法标教授,博士生导师、海南省百人计划、中国科学院青年创新促进会会员。目前核心成员8名。其中研究员/教授1名,副研究员/副教授3名,助理研究员/讲师4名。博士研究生2名,硕士研究生10名。团队人才队伍学科背景互补,学科结构配置互补,集设计研发于一体。研究团队建成了包含分子生物学、化学以及医学影像技术等相结合的较为系统完善的科研平台,并可与学校各实验中心实现高效实验共享,为科研人员创造了便利高效的科研条件。研究所占地1000 m2,启动经费1000万元,科研仪器启动经费1100万元。实验室配备:HITACHI-HT7800透射-扫描电镜、inViaTMQontorTM共焦显微拉曼光谱仪、奥林巴斯超分辨FV3000共聚焦显微镜、徕卡SP8WLL白激光共聚焦显微镜、奥林巴斯FV1000激光共聚焦显微镜、冷泉港小动物活体三维多模式成像系统、HORIBA动态光散射仪、FluoroMax-4/PLUS荧光光谱仪、Lambda 950紫外-可见分光光度计、安捷伦制备液相色谱仪和流式细胞仪等大型仪器。
主要研究领域
瞄准精准医学领域发展前沿,基于光学探针和生物材料的研发,整合(荧光/拉曼/核磁)多模态成像,在肿瘤等疾病可视化影像检测与精准治疗方面开展深入系统的研究。
1)疾病诊断和治疗。基于化学材料,构建分子/纳米影像探针,精准标记肿瘤等疾病病灶,通过成像,在细胞和活体层次上直接观察药物治疗过程中病理生理变化和特征,实现肿瘤等疾病的早期诊断和治疗。
2)药物研发。通过设计特异性探针,利用影像学分析系统,对药物治疗靶点的分子改变成像,直接评价药理作用,大大加快药物的筛选和开发。
3)光学影像手术导航。发展基于有机小分子/纳米材料的探针,整合多种影像优势,利用个性化的精准治疗手段,精确定位肿瘤边界,减少创伤,改善预后。
团队研究成果
相关成果发表在Journal of the American Chemical Society, Chemical Society Reviews, Advanced Functional Materials, Biomaterials, Analytical Chemistry, Chemical Science, Theranostics, Chemical Communications, Biosensors and Bioelectronics, Chemistry-A European Journal, Trends in Analytical Chemistry, Journal of Material Chemistry A 等SCI 期刊80余篇。IF最高40.182。授权专利发明4 项。
于法标
http://www.x-mol.com/university/faculty/49833
课题组网站
http://www.x-mol.com/people/yufabiao
http://bbs.sciencenet.cn/forum.php?mod=group&fid=979
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号