抗癌助手就在你肚子里:《Science》两文揭示共生菌落新角色
长期以来,癌症都是人类的大敌,从小分子化学药物到单抗等生物药物,科学家们一直都在竭尽全力地寻求征服癌症的利器。最近几年,基于激活人体免疫系统的生物疗法,借助体内本已存在的复杂而又强大的天然防御体系来对抗癌症的免疫疗法,取得了喜人的进展。
其中最引人注目的大概就是针对免疫细胞的CTLA-4和PD-1信号通路这两种免疫疗法靶点。在免疫系统中,作为正规军主力部队的T细胞,在识别癌细胞、直接杀死癌细胞以及组织免疫系统其它武装力量来歼灭肿瘤等方面,具有举足轻重的作用。正如同汽车必须有刹车以防止其行驶失控一样,对T细胞来说,也有类似的“刹车”调控机制,CTLA-4和PD-1信号通路就正是这样的防止T细胞失控并伤害自身组织的机制。而肿瘤细胞也正是利用了这种机制,通过激活这两种被称为“免疫检查站(checkpoint)”的受体,来逃避T细胞的追杀。针对CTLA-4和PD-1的免疫疗法,正是要抑制这两种“免疫检查站”的作用,使T细胞恢复癌细胞杀手的威力。市场上的单抗药物ipilimumab就是针对CTLA-4通路,而nivolumab和pembrolizumab则是针对PD-1通路的免疫药物。
尽管这种免疫疗法在一些癌症患者身上取得了可喜的效果,检查站抑制剂(checkpoint inhibitors)可以通过缩小肿瘤来延长患者的生命,有的患者的生存期甚至延长了好几年。但是同样的疗法对于其他很大一部分患者却效果不佳。比如有20%的使用了ipilimumab的黑色素瘤患者的生存期延长了,但科学家不知道为什么另外80%的患者却没有有效反应。
来自法国和美国的两个科学家小组最近在《Science》上发表了两篇文章,通过小鼠实验揭示了一个令人惊讶的原因:这些对免疫治疗无效的患者,可能在其肠道里没有合适的微生物群落。这两项研究都表明,肠道共生菌的组成,可以决定这些针对癌症的免疫疗法是否有效。
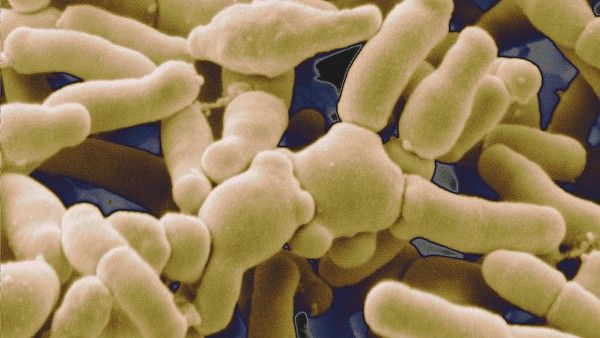
双歧杆菌能够刺激免疫系统对抗肿瘤细胞。图片来源:Scimat/Science Source
这些研究成果首次揭示了肠道共生菌与检查站抑制剂疗效的关联,极有可能改变医生使用抗癌药物的策略。“这两篇论文都令人信服地表明,(肠道)微生物会影响治疗,”美国国家健康研究院下属的过敏和传染病研究所的免疫学专家Yasmine Belkaid评论说。在过去,研究人员通常期望通过寻找患者的基因组中可能的突变来解释为什么一个特定的检查站抑制剂是无效的,北卡罗莱纳大学教堂山分校的分子生物学家Scott Bultman说。新的结果是令人鼓舞的,他说,因为“与改变你的基因组相比,改变你的肠道菌群更容易。”
对于法国科学家Laurence Zitvogel及其同事来说,对肠道微生物的关注源于研究免疫药物出现的副作用。ipilimumab经常会引发结肠炎,这是一种发生于大肠的炎症,这里也是肠道共生菌的一个重要栖息地。这种副作用表明检查点抑制剂和微生物可能有相互作用。作为对这种可能性的进一步研究,研究人员追踪了植入性肿瘤在缺乏肠道细菌的小鼠体内的增长。

Laurence Zitvogel(中) 图片来源:leparisien.fr
Zitvogel和同事们的进一步研究分析表明,某些杆菌和伯克霍尔德属的细菌决定了抗肿瘤效果。为了确认这种可能性,研究人员将这些特殊的微生物送入无肠道细菌的小鼠体内,方法是直接喂食微生物或给它们喂食一些经ipilimumab治疗的患者的富集杆菌的粪便。在这两种情况下,这些微生物的大量进入都加强了小鼠对于检查站抑制剂的响应。“已经在我们肠道中的万亿细菌,可以把我们的免疫系统调动起来,”Zitvogel说。
美国芝加哥大学的免疫学家Thomas Gajewski和同事们则是通过比较来自不同供应商的小鼠体内肿瘤的差异得到类似的结论。他们发现,在分别来自于Jackson Laboratory和Taconic Farms的小鼠中,黑色素瘤在前者体内的增长慢于后者。由于这些小鼠在同一笼中时会互相吃掉对方的排泄物,其体内微生物组会趋向于同质化。这些研究人员将来自这两个供应商的小鼠混在同一个笼子里后,发现其肿瘤生长速度的差异消失了。这表明这些动物的肠道微生物的类型确实对肿瘤生长有影响。

Thomas Gajewski 图片来源:UCM
当他们分析了这些小鼠的微生物组后,研究人员明确找出了一种称为双歧杆菌的细菌种类。研究小组发现,对Taconic Farms的小鼠喂食含有几种双歧杆菌的益生菌能够增加抗肿瘤的检查站抑制剂的疗效。“共生细菌显著影响内源性抗肿瘤反应”,文章作者之一Ayelet Sivan说。
这两个团队的研究涉及了不同的细菌种类,但来自于佛罗里达大学的微生物免疫学家Christian Jobin对此并不介意。“不同的药物,不同的微生物,但同样的终点,”他说。他还补充说,这些研究结果也是对2013年的两项研究的补充,那些研究表明微生物会影响化疗的效果。
这一发现“开辟了增强抗癌疗效的新方式,”美国约翰霍普金斯大学的传染病专家Cynthia Sears说。例如,有可能用益生菌来加强患者的抗肿瘤反应。不过,研究人员也看到一些潜在的障碍。正如Zitvogel指出的,美国和欧洲的监管机构还没有批准对癌症患者使用微生态制剂;而且目前微生物是如何促进免疫应答的机理还有待进一步研究。“目前还不清楚我们是否可以有意义的操纵微生物来对健康创造积极的影响,”Sears说。不过,这些研究表明,我们可能在对抗癌症的斗争中找到了一些功能强大的新盟友。
1. http://www.sciencemag.org/content/early/2015/11/09/science.aac4255.abstract
2. http://www.sciencemag.org/content/early/2015/11/04/science.aad1329.abstract
3. http://news.sciencemag.org/biology/2015/11/gut-microbes-give-anticancer-treatments-boost
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号