Science:前方“高能”!生物催化轻松解决有机合成难题
进化是生物种群通过适应生存环境得以繁衍的最基本手段。“定向进化”,这一概念在上世纪90年代由美国加州理工学院(Caltech)的Frances Arnold教授(点击查看介绍)提出,通过模拟生物学上的进化,实现在人工筛选下对生物个体基因序列的迅速改写以达到所预期的表现形式或者功能状态。如今,定向进化这一策略被广泛应用于生物以及生物交叉领域的各个分支,尤其在酶工程这一方向上,有着无可替代的重要意义。酶在生物体内催化着各式各样的化学反应,这样的功能是生物体为满足自身需求在进化过程中对环境的响应。然而,从化学家的角度,正是因为酶的功能有如此强的目的性,才使得酶这种生物催化剂特点鲜明:高效、特异但往往缺乏普适性。定向进化通过改造酶所对应的基因序列,在酶的工程化中平衡了酶的各类性质,极大程度的拓宽了生物催化的潜力,使之能拥有广泛的底物普适性,甚至催化全新的化学反应。
近年来,Frances Arnold教授课题组一系列高质量的工作也正向人们展现着生物催化的广泛前景,以及定向进化策略所展现的无可比拟的作用。其中的代表性工作有:细胞色素c 用于碳硅键的构筑(Science, 2016, 354, 1048,点击阅读详细)和碳硼键的形成(Nature, 2017, 552, 7683,点击阅读详细),细胞色素P450用于烯烃的反马氏氧化(Science, 2017, 358, 215,点击阅读详细)和碳氢氨基化反应(Nat. Chem., 2017, 9, 627,点击阅读详细)。

Frances Arnold教授。图片来源:California Institute of Technology
上周,Frances Arnold教授课题组再次报道了令人惊叹的工作。该团队对细胞色素P450的酶系列做了进一步的定向进化,使之能够轻松、简洁、大量地合成传统有机合成实验室难以合成的高张力有机碳环体系——双环丁烷(bicyclo[1.1.0]butane)和环丙烯(cyclopropene)。斯坦福大学的Carolyn Bertozzi教授评价道,“当众人都已无法想象酶还有什么能比目前化学做得更好的,他们依旧能突破屏障,让人瞠目结舌!”相关工作发表在Science上,博士生陈凯(Kai Chen)为该工作的第一作者。

由酶合成高张力碳环分子。图片来源:California Institute of Technology
有机化学中,小环化合物往往由于键角键长的扭曲以及取代基在空间上的堆积碰撞,使得它们包含了张力能。环丙烷、环丁烷作为最小的碳环,拥有26‒28 kcal/mol的张力能。然而在这些小环中,进一步引入不饱和键或者碳桥,将导致张力能的进一步提升。比如,环丙烯的张力能在54 kcal/mol左右,而双环丁烷更达到66 kcal/mol。也正是因为如此之高的张力能,让这些小环作为中间体在合成化学、材料化学中有着广泛应用。比如,双环丁烷在受到特定的外源刺激时能释放张力能,并且自身形成共轭双烯结构;这一性质在它作为单体被用在应激高分子材料中时,使应激过程伴随导电性、光学性质等物理性质的改变。
然而,这样高的张力能也使得制备这些小环的难度超乎想象。双环丁烷的合成往往依赖于有机锂试剂作用下溴乙基二溴环丙烷的分子内还原性偶联,或者是两分子的卡宾加成到碳碳叁键。有机锂试剂的危险性毋用多说,第二种方法也仅仅局限于非取代的亚甲基卡宾。多取代双环丁烷的不对称合成更是难上加难,迄今为止鲜有报道。在生物体系中,虽然各类酶催化合成形式各样的天然产物,其中也不乏一些含环丙烷的天然分子,但是环丙烯或者双环丁烷的结构却是少之又少,可能由于生物体系中缺乏这样碳环的合成机制,也或许是这些高张力的结构在生物环境中并不能稳定存在。
基于该课题组早期的工作——用细胞色素P450催化烯烃的环丙烷化(Science, 2013, 339, 307),作者设想或许可以把类似的卡宾机制应用在炔烃上,如此一来,一分子的卡宾加成得到环丙烯,若能再继续转移一分子卡宾则能得到双环丁烷。这个看似非常简单的设想,却存在诸多挑战:(1)或许第一步的卡宾加成对其他过渡金属催化剂是可行的,但对酶而言能否实现尚不可知;(2)即便能完成第一步,得到的环丙烯是蕴含高能量的中间体,或许需要酶稳定其结构以避免副反应的发生;(3)第二步卡宾加成,除了最简单的亚甲基卡宾之外几乎鲜有报道,然而对于α-取代的卡宾而言,取代基位阻势必会大幅增加其难度;(4)最后,两步的卡宾加成对酶而言,相当于需要接纳两类不同的底物,而且都需要有非常好的立体控制才能得到高立体专一性的双环丁烷。这种种的难度,或许也是传统催化发展至今也未见一例通过两分子卡宾加成到叁键来合成不对称双环丁烷的原因吧。
但作者相信,通过调节酶内部的活性中心结构,或许可以构建一个合适的环境用于高效的结合底物、稳定中间体以及诱导强有力的立体控制,从而实现两类高张力碳环的构建。一开始,以苯乙炔和2-重氮乙酸乙酯(EDA)为底物,作者尝试了血红素以及多种基于血红素的蛋白作为反应催化剂,包括细胞色素P450、P411(P450中铁原子的轴向配体氨基酸由Cys替换为Ser)、细胞素色c、血红蛋白以及其他的球蛋白。然而,没有一个蛋白能催化预期的反应,给出了环丙烯或者双环丁烷的产物。有趣的是,P411-S1 I263W突变体给出了一个呋喃结构的产物。动力学实验发现该呋喃产物由环丙烯重排得到,这说明了P411蛋白能够催化卡宾加成到叁键,尽管此前从未有铁催化剂或者酶被报道过拥有这一性质。但这也暗示了这类环丙烯中间体是高度不稳定的,若不能及时转移第二个卡宾,只能得到相应的副产物。
在这之后的一系列尝试中,作者发现在蛋白结构中位于血红素辅酶正上方的263位点能有效控制卡宾加成的过程。在此基础上,增加数个活性中心突变后的P411-P4突变体,以80 的催化转化数(TTN)生成了双环丁烷的产物;再加以数个突变后,P411-E10突变体的TTN达到了530,提高6倍之多。而且通过核磁手段,作者也确定了产物结构是exo, endo 形式的构象,而不是exo, exo 或endo, endo 构象的内消旋体。基于这些发现,作者想通过“定向进化”策略进一步提高蛋白的催化性能,针对活性位点附近的氨基酸残基进行数轮进化之后,E10 V78F S438A突变体的TTN高达1880。
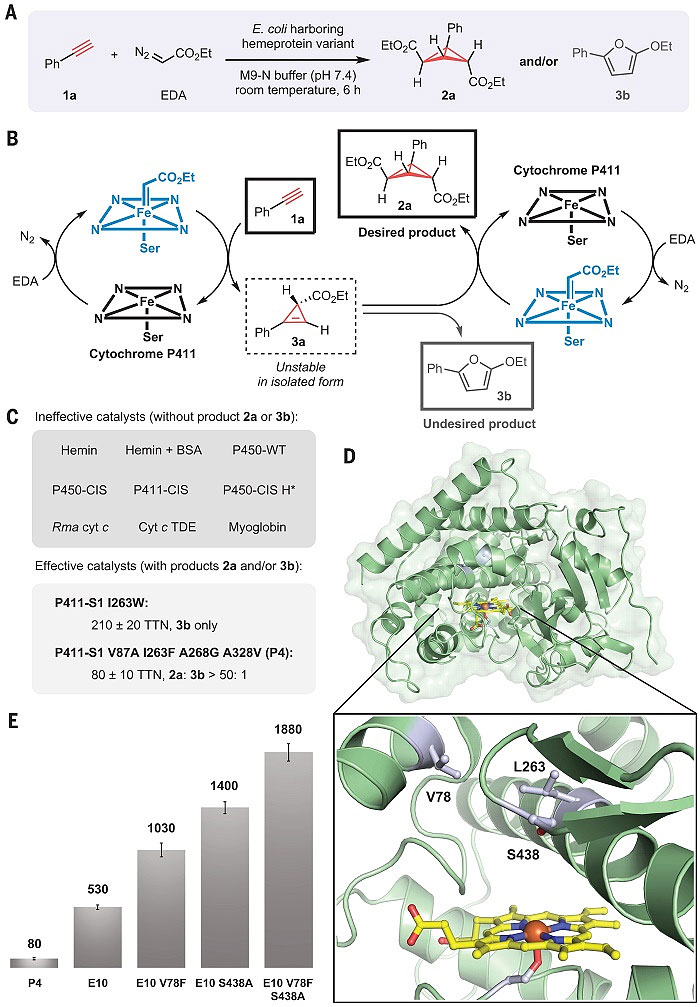
图1. 血红素蛋白催化的双环丁烷合成。A. 反应式. B. 催化循环. C. 蛋白筛选. D. P411-E10蛋白结构. E. 定向进化。图片来源:Science
之后,作者研究了在进化得到的突变体催化下双环丁烷化的底物范围。一系列芳香炔都能顺利的被转化为双环丁烷产物,其中数个底物还能用于毫摩尔级别的放大量合成。所有底物都实现了较高的TTN(最高可达1760)以及较好的分离收率(最高可达80%)。然而,由于此前文献中未有任何传统催化手段实现该反应,这使得作者不能以常规手段来鉴定产物的手性纯度。但作者仍以手性衍生化的方式说明了双环丁烷2l和2m应该具有很高的手性纯度——衍生化产物4b和4c仅观测到一种非对映异构体。除此之外,酯基还原反应得到相应的二醇产物4d,也使得作者能最终确定双环丁烷的绝对构型。
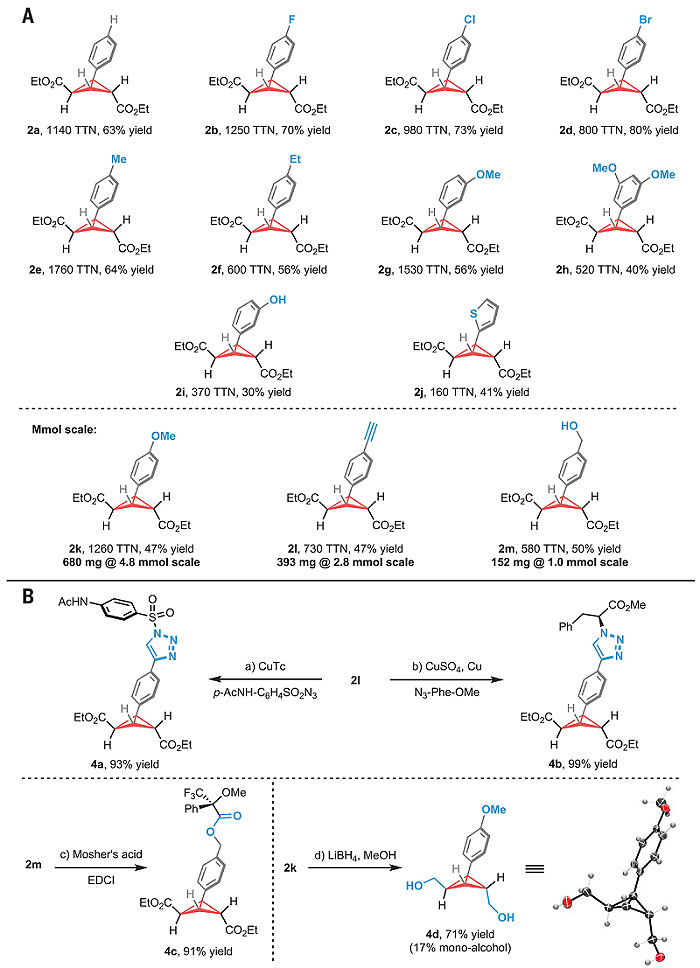
图2. A. 双环丁烷化底物范围. B. 双环丁烷产物的衍生化。图片来源:Science
接下来,作者发现如果用脂肪炔作为底物,反应便可以停在环丙烯,且该类环丙烯具有较好的稳定性。在经过一系列初始筛选之后,P411-P4突变体能以260 TTN催化4-苯丁炔环丙烯化,并实现较高的立体选择性(95.5:4.5 e.r.)。对该突变体中的87位点的残基进行饱和突变后,得到A87F和A87W两个突变,拥有截然相反的立体选择性(3.0:97.0 e.r. 和97.1:2.9 e.r.),这说明了该位点具有底物识别功能,且能参与底物构象控制。以这两个突变体为起始点,数轮进化给出了两个最终突变体P411-C6和K10,能将催化效率提高到10倍以上并实现几乎单一的手性控制(99.55:0.45 和 99.95:0.05 e.r.,对应S 和R 构型)。同样,环丙烯化也拥有非常广的底物范围,对于13个不同的底物都给出了数百到数千的TTN、较高的手性选择性以及分离产率。后续衍生化也展示了环丙烯可用于复杂环丙烷或者双环体系的合成。
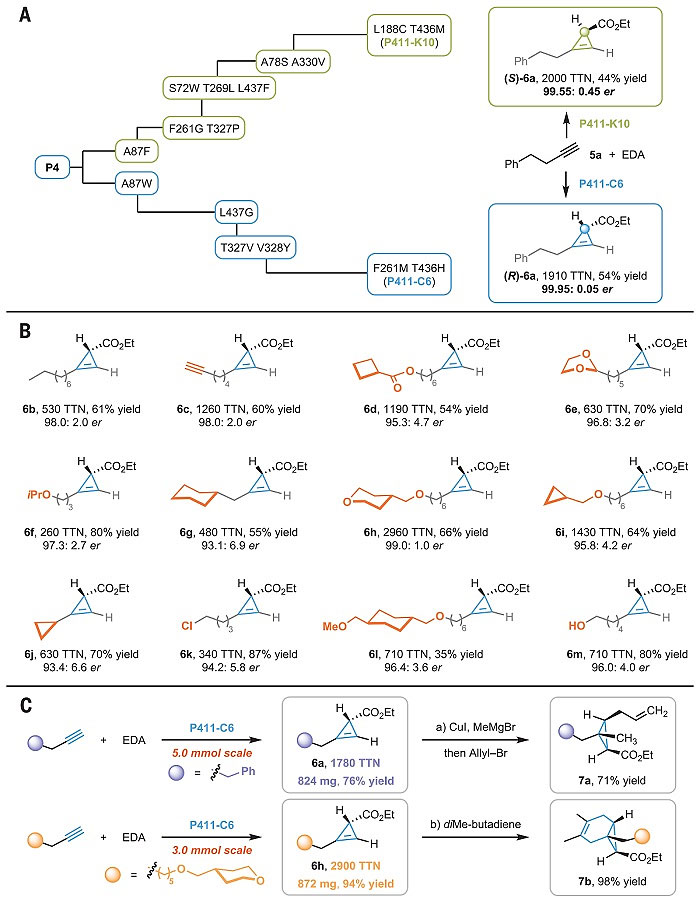
图3. A. 定向进化. B. 环丙烯化底物范围. C. 放大量合成与衍生化. 图片来源:Science.
——总结——
Frances Arnold教授课题组这一最新工作充分展现了生物催化的强大潜力。以蛋白功能为导向,只需要数轮的进化,细胞色素P411一系列酶能被快速改造用于高效合成极具张力的双环丁烷和环丙烯结构。较之传统小分子催化剂,蛋白的独特之处也得以全面的展现:能够高效结合底物以降低反应的活化能垒,能通过弱相互作用稳定高活性的中间体,以及能够精准的控制底物的构象以实现立体专一性。也正因为解决了这些问题,进化后的P411突变体才能高效的实现手性双环丁烷合成,得以大幅超越传统催化方法。在基因手段的辅助下,蛋白能够被轻松改造,其快速、便捷、可调控、易改写的性能,终将使生物催化在合成化学领域之中,占得不可替代的一席之地。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Enzymatic construction of highly strained carbocycles
Science, 2018, 360, 71-75, DOI: 10.1126/science.aar4239
导师介绍
Frances Arnold
http://www.x-mol.com/university/faculty/438
(非常感谢论文作者对本报道的支持!)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号